
题目列表(包括答案和解析)
(6分)PCl5的热分解反应如下:PCl5(g) 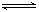 PCl3(g) + Cl2(g)。
PCl3(g) + Cl2(g)。
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150mol/L。求该温度下的平衡常数。
(3)在相同的容器中起始充入5.00mol PCl5,达平衡后, PCl5的分解率是多少?
(6分)PCl5的热分解反应如下:PCl5(g) 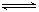 PCl3(g)
+ Cl2(g)。
PCl3(g)
+ Cl2(g)。
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150mol/L。求该温度下的平衡常数。
(3)在相同的容器中起始充入5.00mol PCl5,达平衡后, PCl5的分解率是多少?
 PCl3(g) + Cl2(g)。
PCl3(g) + Cl2(g)。PCl5的热分解反应如下:PCl5(g)![]() PCl3(g)+Cl2(g).
PCl3(g)+Cl2(g).
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0 L的密闭容器中充入2.00 mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150 mol/L.计算该温度下的平衡常数.
PCl5的热分解反应如下:PCl5(g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0 L的密闭容器中充入2.00 mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150 mol/L.计算该温度下的平衡常数.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com