
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
(15·Ц)ДЬФҙКЗ№ъГсҫӯјГ·ўХ№өДЦШТӘ»щҙЎЈ¬ОТ№ъДҝЗ°К№УГөДДЬФҙЦчТӘКЗ»ҜКҜИјБПЎЈ
(1)ФЪ25ЎжЎў101 kPaКұЈ¬16 g CH4НкИ«ИјЙХЙъіЙТәМ¬Л®Кұ·ЕіцөДИИБҝКЗ890.31 kJЈ¬ФтCH4ИјЙХөДИИ»ҜС§·ҪіМКҪОӘ__________________________________________ЎЈ
(2)ТСЦӘЈәC(s)Ј«O2(g)===CO2(g)Ј»ҰӨHЈҪЈӯ437.3 kJЎӨmolЈӯ1
H2(g)Ј«O2(g)===H2O(g)Ј»ҰӨHЈҪЈӯ285.8 kJЎӨmolЈӯ1
CO(g)Ј«O2(g)===CO2(g)Ј»ҰӨHЈҪЈӯ283.0 kJЎӨmolЈӯ1
ФтГәЖш»Ҝ·ҙУҰC(s)Ј«H2O(g)===CO(g)Ј«H2(g) өДмКұдҰӨHЈҪ________kJЎӨmolЈӯ1ЎЈ
ЈЁ3Ј©ИзПВНјЛщКҫЧйіЙұХәП»ШВ·Ј¬ЖдЦРЈ¬јЧЧ°ЦГЦРCH4ОӘёәј«Ј¬O2әНCO2өД»мәПЖшМеОӘХэј«Ј¬ПЎНБҪрКфІДБПОӘөзј«Ј¬ТФИЫИЪМјЛбСООӘөзҪвЦКЈ»ТТЧ°ЦГЦРaЎўbОӘКҜД«Ј¬bј«ЙПУРәмЙ«ОпЦКОціцЈ¬CuSO4ИЬТәөДМе»эОӘ200 mLЎЈ

ўЩјЧЧ°ЦГЦРЖшМеAОӘ ЈЁМоЎ°CH4Ўұ»тЎ°O2әНCO2ЎұЈ©Ј¬dј«ЙПөДөзј«·ҙУҰКҪОӘ_____________ЎЈ
ўЪТТЧ°ЦГЦРaј«ЙПөДөзј«·ҙУҰКҪОӘ____________________________ЎЈ
ИфФЪaј«ІъЙъ112mL(ұкЧјЧҙҝц)ЖшМеЈ¬ФтјЧЧ°ЦГЦРПыәДCH4________ mL (ұкЧјЧҙҝц)Ј¬ТТЧ°ЦГЦРЛщөГИЬТәөДpH=__________ЎЈЈЁәцВФөзҪвЗ°әуИЬТәМе»эұд»ҜЈ©
ўЫИз№ыТТЦРөзј«І»ұдЈ¬Ҫ«ИЬТә»»іЙұҘәНNa2SO4ИЬТәЈ¬өұТхј«ЙПУРa molЖшМеЙъіЙКұЈ¬Н¬КұУРw g Na2SO4ЎӨ10H2Oҫ§МеОціцЈ¬ИфОВ¶ИІ»ұдЈ¬КЈУаИЬТәЦРИЬЦКөДЦКБҝ·ЦКэУҰОӘ________(УГә¬wЎўaөДұнҙпКҪұнКҫЈ¬І»ұШ»Ҝјт)ЎЈ
ЈЁ№І16·ЦЈ¬Г»ҝХ2·ЦЈ©
ТСЦӘПВБРИИ»ҜС§·ҪіМКҪЈә
ўЩC(s)Ј«H2O(s)===CO(g)Ј«H2(g) ҰӨHЈҪЈӯ131.3 kJЎӨmolЈӯ1
ўЪH2SO4(l)Ј«NaOH(l)===Na2SO4(l)Ј«H2O(l)ЎЎ ҰӨHЈҪЈӯ57.3 kJЎӨmolЈӯ1
ўЫC(s)Ј«O2(g)===CO2(g) ҰӨHЈҪЈӯ393.5 kJЎӨmolЈӯ1
ўЬCO(g)Ј«O2(g)===CO2(g) ҰӨHЈҪЈӯ283 kJЎӨmolЈӯ1
ўЭHNO3(aq)Ј«NaOH(aq)===NaNO3(aq)Ј«H2O(l) ҰӨHЈҪЈӯ57.3 kJЎӨmolЈӯ1
ўЮH2(g)+ O2(g)===H2O(1)
ҰӨH=Јӯ285.6kJ/mol
O2(g)===H2O(1)
ҰӨH=Јӯ285.6kJ/mol
ўЯC3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) ҰӨH=Јӯ2220.0 kJЎӨmolЈӯ1
ўа N2 (g)+ 3H2(g) === 2NH3 (g) ҰӨH=Јӯ92 kJЎӨmolЈӯ1
ЈЁ1Ј©ЙПКцИИ»ҜС§·ҪіМКҪЦРЈ¬І»ХэИ·өДУР______________Ј¬І»ХэИ·өДАнУЙ·ЦұрКЗ _____________________________________________________________________________ЎЈ
(2)ёщҫЭЙПКцРЕПўЈ¬РҙіцCЧӘ»ҜОӘCOөДИИ»ҜС§·ҪіМКҪЈә______________________ЎЈ
(3)КөСйІвөГH2әНC3H8өД»мәПЖшМе№І5molЈ¬НкИ«ИјЙХЙъіЙТәМ¬Л®Кұ·ЕИИ6262.5kJ,Фт»мәПЖшМеЦРH2әНC3H8өДМе»эұИКЗ ЎЈ
(4)ТСЦӘЈәH2O(1)=H2O(g)Ј»ҰӨH=+44.0kJ/molРҙіцұыНйИјЙХЙъіЙCO2әНЖшМ¬Л®өДИИ»ҜС§·ҪіМКҪ
(5)ЙПКц·ҙУҰЦРЈ¬ұнКҫИјЙХИИөДИИ»ҜС§·ҪіМКҪУР__________________________________Ј»
ұнКҫЦРәНИИөДИИ»ҜС§·ҪіМКҪУР______________ЎЈ
(6) ТСЦӘHЎӘHјьДЬОӘ436 kJ/molЈ¬HЎӘNјьДЬОӘ391kJ/molЈ¬ФтNЎФNјьөДјьДЬКЗ_____________Јҝ
ЈЁ16·ЦЈ¬ГҝҝХ2·ЦЈ©ТСЦӘ·ЗҪрКфөҘЦКБтЈЁSЈ©КЗөӯ»ЖЙ«№ММе·ЫД©Ј¬ДСИЬУЪЛ®ЎЈОӘБЛСйЦӨВИФӘЛШөД·ЗҪрКфРФұИБтФӘЛШөД·ЗҪрКфРФЗҝЈ¬Ді»ҜС§КөСйРЎЧйЙијЖБЛИзПВКөСйЈ¬Зл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©Ч°ЦГAөД·ЦТәВ©¶·ЦРКўЧ°өДКФјБКЗ Ј¬ЙХЖҝЦРөД»ҜС§·ҙУҰ·ҪіМКҪ ЎЈ
ЈЁ2Ј©Ч°ЦГBЛщјУКФјБұҘәНNaClИЬТәЈ¬ЖдЧ°ЦГөДЧчУГКЗ ЎЈ
ЈЁ3Ј©Ч°ЦГCЦРКў·ЕөДКФјБКЗ ЈЁСЎМоПВБРЛщёшКФјБөДҙъВлЈ©Ј¬КөСйПЦПуОӘ Ј¬
ёГ·ҙУҰөДАлЧУ·ҪіМКҪКЗ ЎЈ
AЈ®Na2SИЬТә BЈ®Na2SO3ИЬТә CЈ®Na2SO4ИЬТә
(4Ј©ТСЦӘЈәўЩБтЛбұИҙОВИЛбОИ¶ЁЈ»ўЪёЯВИЛбұИБтЛбЛбРФЗҝЈ»ўЫS2-ұИCl-ТЧұ»Сх»ҜЈ»ўЬHClұИH2SОИ¶ЁЈ»ўЭНӯУлСОЛбІ»·ҙУҰЈ¬ө«ДЬУлЕЁБтЛб·ҙУҰЈ»ўЮМъУлВИЖшјУИИЙъіЙИэВИ»ҜМъЈ¬МъУлБтјУИИЙъіЙБт»ҜСЗМъЈ»ўЯБтФӯЧУУлВИФӯЧУөзЧУІгКэПаН¬Ј¬ВИФӯЧУ°лҫ¶РЎУЪБтФӯЧУЎЈҝЙЛөГчВИұИБт·ЗҪрКфРФЗҝөДКЗ
AЈ®И«Іҝ BЈ®ўЪўЫўЬўЮўЯ CЈ®ўЩўЪўЬўЭўЮ DЈ®іэўЩТФНв
ЈЁ5Ј©Ч°ЦГDЦРКў·ЕЙХјоИЬТәЈ¬ДҝөДКЗОьКХ·ҙУҰәуКЈУаөДЖшМеЈ¬·АЦ№ОЫИҫҝХЖшЈ¬Рҙіц·ҙУҰөДАлЧУ·ҪіМКҪ ЎЈ
(13·Ц)ўс.Т»Сх»ҜМјКЗТ»ЦЦУГНҫПаөұ№г·әөД»Ҝ№Ө»щҙЎФӯБПЎЈ
(1)АыУГПВБР·ҙУҰҝЙТФҪ«ҙЦДшЧӘ»ҜОӘҙҝ¶Иҙп99.9%өДёЯҙҝДшЎЈ
Ni(s)Ј«4CO(g) Ni(CO)4(g) ёГ·ҙУҰөДҰӨH Ўш 0 (СЎМоЎ°ЈҫЎұ»тЎ°ЈҪЎұ»тЎ°ЈјЎұ)ЎЈ
Ni(CO)4(g) ёГ·ҙУҰөДҰӨH Ўш 0 (СЎМоЎ°ЈҫЎұ»тЎ°ЈҪЎұ»тЎ°ЈјЎұ)ЎЈ
(2)ФЪёЯОВПВТ»Сх»ҜМјҝЙҪ«¶юСх»ҜБт»№ФӯОӘөҘЦКБтЎЈТСЦӘЈә
C(s)Ј«O2(g)ЈҪCO2(g) ҰӨH1ЈҪЈӯ393.5 kJЎӨmolЈӯ1
CO2(g)Ј«C(s)ЈҪ2CO(g) ҰӨH2ЈҪ+ 172.5 kJЎӨmolЈӯ1
S(s)Ј«O2(g)ЈҪSO2(g) ҰӨH3ЈҪЈӯ296.0 kJЎӨmolЈӯ1
ЗлРҙіцCOіэSO2өДИИ»ҜС§·ҪіМКҪ Ўш ЎЈ
(3)ПВНјЦРЧуНјКЗТ»МјЛбСОИјБПөзіШЈ¬ЛьТФCOОӘИјБПЈ¬Т»¶ЁұИАэLi2CO3әНNa2CO3өНИЫ»мәПОпОӘөзҪвЦКЈ¬УТНјКЗҙЦНӯҫ«Б¶өДЧ°ЦГНјЈ¬ПЦУГИјБПөзіШОӘөзФҙҪшРРҙЦНӯөДҫ«Б¶КөСйЎЈ»ШҙрПВБРОКМвЈә
ўЩРҙіцAј«·ўЙъөДөзј«·ҙУҰКҪ Ўш ЎЈ
ўЪТӘУГИјБПөзіШОӘөзФҙҪшРРҙЦНӯөДҫ«Б¶КөСйЈ¬ФтBј«УҰёГУлЎш ј«(МоЈәЎ°CЎұ»тЎ°DЎұ)ПаБ¬ЎЈ
ўЫөұПыәД2.24 L(ұкҝцПВ)COКұЈ¬ҙЦНӯөзј«АнВЫЙПјхЙЩНӯөДЦКБҝ Ўш (МоЈәЎ°ҙуУЪЎұЎўЎ°өИУЪЎұ »тЎ°РЎУЪЎұ)6.4ҝЛЎЈ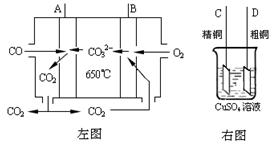
ўт.(1)ТСЦӘNa2CrO4ИЬТәЛб»ҜКұ·ўЙъөД·ҙУҰОӘЈә2CrO42ЈӯЈ«2HЈ« Cr2O72ЈӯЈ«H2OЈ¬Иф1LЛб»ҜәуЛщөГИЬТәЦРёхФӘЛШөДЧЬОпЦКөДБҝОӘ0.55 molЈ¬CrO42ЈӯУР10/11ЧӘ»ҜОӘCr2O72ЈӯЎЈУЦЦӘЈәіЈОВКұёГ·ҙУҰөДЖҪәвіЈКэKЈҪ1014ЎЈЙПКцЛб»ҜәуЛщөГИЬТәөДpHЈҪ Ўш ЎЈ
Cr2O72ЈӯЈ«H2OЈ¬Иф1LЛб»ҜәуЛщөГИЬТәЦРёхФӘЛШөДЧЬОпЦКөДБҝОӘ0.55 molЈ¬CrO42ЈӯУР10/11ЧӘ»ҜОӘCr2O72ЈӯЎЈУЦЦӘЈәіЈОВКұёГ·ҙУҰөДЖҪәвіЈКэKЈҪ1014ЎЈЙПКцЛб»ҜәуЛщөГИЬТәөДpHЈҪ Ўш ЎЈ
(2)ёщҫЭУР№Ш№ъјТұкЧјЈ¬ә¬CrO42ЈӯөД·ПЛ®ТӘҫӯ»ҜС§ҙҰАнЈ¬К№ЖдЕЁ¶ИҪөЦБ5.0ЎБ10Јӯ7 molЎӨLЈӯ1ТФПВІЕДЬЕЕ·ЕЎЈә¬CrO42ЈӯөД·ПЛ®ҙҰАнНЁіЈУРТФПВБҪЦЦ·Ҫ·ЁЎЈ
ўЩіБөн·ЁЈәјУИлҝЙИЬРФұөСОЙъіЙBaCrO4іБөнЈЫKsp(BaCrO4)ЈҪ1.2ЎБ10Јӯ10ЈЭЈ¬ФЩјУИлҝЙИЬРФБтЛбСОҙҰАн¶аУаөДBa2Ј«ЎЈјУИлҝЙИЬРФұөСОәуөД·ПЛ®ЦРBa2Ј«өДЕЁ¶ИУҰІ»РЎУЪ Ўш molЎӨLЈӯ1Ј¬И»әуФЩҪшРРәуРшҙҰАн·ҪДЬҙпөҪ№ъјТЕЕ·ЕұкЧјЎЈ
ўЪ»№Фӯ·ЁЈәCrO42Јӯ Cr3Ј«
Cr3Ј« Cr(OH)3ЎЈУГёГ·Ҫ·ЁҙҰАн10 m3 CrO42ЈӯөДОпЦКөДБҝЕЁ¶ИОӘ1.0ЎБ10ЎӘ3 molЎӨLЈӯ1өД·ПЛ®Ј¬ЦБЙЩРиТӘВМ·Ҝ(FeSO4ЎӨ7H2OЈ¬Па¶Ф·ЦЧУЦКБҝОӘ278) Ўш Kg(ұЈБфБҪО»РЎКэ)ЎЈ
Cr(OH)3ЎЈУГёГ·Ҫ·ЁҙҰАн10 m3 CrO42ЈӯөДОпЦКөДБҝЕЁ¶ИОӘ1.0ЎБ10ЎӘ3 molЎӨLЈӯ1өД·ПЛ®Ј¬ЦБЙЩРиТӘВМ·Ҝ(FeSO4ЎӨ7H2OЈ¬Па¶Ф·ЦЧУЦКБҝОӘ278) Ўш Kg(ұЈБфБҪО»РЎКэ)ЎЈ
(13·Ц)ўс.Т»Сх»ҜМјКЗТ»ЦЦУГНҫПаөұ№г·әөД»Ҝ№Ө»щҙЎФӯБПЎЈ
(1)АыУГПВБР·ҙУҰҝЙТФҪ«ҙЦДшЧӘ»ҜОӘҙҝ¶Иҙп99.9%өДёЯҙҝДшЎЈ
Ni(s)Ј«4CO(g)Ni(CO)4(g) ёГ·ҙУҰөДҰӨH Ўш 0 (СЎМоЎ°ЈҫЎұ»тЎ°ЈҪЎұ»тЎ°ЈјЎұ)ЎЈ
(2)ФЪёЯОВПВТ»Сх»ҜМјҝЙҪ«¶юСх»ҜБт»№ФӯОӘөҘЦКБтЎЈТСЦӘЈә
C(s)Ј«O2(g)ЈҪCO2(g) ҰӨH1ЈҪЈӯ393.5 kJЎӨmolЈӯ1
CO2(g)Ј«C(s)ЈҪ2CO(g) ҰӨH2ЈҪ+ 172.5 kJЎӨmolЈӯ1
S(s)Ј«O2(g)ЈҪSO2(g) ҰӨH3ЈҪЈӯ296.0 kJЎӨmolЈӯ1
ЗлРҙіцCOіэSO2өДИИ»ҜС§·ҪіМКҪ Ўш ЎЈ
(3)ПВНјЦРЧуНјКЗТ»МјЛбСОИјБПөзіШЈ¬ЛьТФCOОӘИјБПЈ¬Т»¶ЁұИАэLi2CO3әНNa2CO3өНИЫ»мәПОпОӘөзҪвЦКЈ¬УТНјКЗҙЦНӯҫ«Б¶өДЧ°ЦГНјЈ¬ПЦУГИјБПөзіШОӘөзФҙҪшРРҙЦНӯөДҫ«Б¶КөСйЎЈ»ШҙрПВБРОКМвЈә
ўЩРҙіцAј«·ўЙъөДөзј«·ҙУҰКҪ Ўш ЎЈ
ўЪТӘУГИјБПөзіШОӘөзФҙҪшРРҙЦНӯөДҫ«Б¶КөСйЈ¬ФтBј«УҰёГУл Ўш ј« (МоЈәЎ°CЎұ»тЎ°DЎұ)ПаБ¬ЎЈ
ўЫөұПыәД2.24 L(ұкҝцПВ)COКұЈ¬ҙЦНӯөзј«АнВЫЙПјхЙЩНӯөДЦКБҝ Ўш (МоЈәЎ°ҙуУЪЎұЎўЎ°өИУЪЎұ »тЎ°РЎУЪЎұ)6.4ҝЛЎЈ
ўт.(1)ТСЦӘNa2CrO4ИЬТәЛб»ҜКұ·ўЙъөД·ҙУҰОӘЈә2CrO42ЈӯЈ«2HЈ«Cr2O72ЈӯЈ«H2OЈ¬Иф1LЛб»ҜәуЛщөГИЬТәЦРёхФӘЛШөДЧЬОпЦКөДБҝОӘ0.55 molЈ¬CrO42ЈӯУР10/11ЧӘ»ҜОӘCr2O72ЈӯЎЈУЦЦӘЈәіЈОВКұёГ·ҙУҰөДЖҪәвіЈКэKЈҪ1014ЎЈЙПКцЛб»ҜәуЛщөГИЬТәөДpHЈҪ Ўш ЎЈ
(2)ёщҫЭУР№Ш№ъјТұкЧјЈ¬ә¬CrO42ЈӯөД·ПЛ®ТӘҫӯ»ҜС§ҙҰАнЈ¬К№ЖдЕЁ¶ИҪөЦБ5.0ЎБ10Јӯ7 molЎӨLЈӯ1ТФПВІЕДЬЕЕ·ЕЎЈә¬CrO42ЈӯөД·ПЛ®ҙҰАнНЁіЈУРТФПВБҪЦЦ·Ҫ·ЁЎЈ
ўЩіБөн·ЁЈәјУИлҝЙИЬРФұөСОЙъіЙBaCrO4іБөнЈЫKsp(BaCrO4)ЈҪ1.2ЎБ10Јӯ10ЈЭЈ¬ФЩјУИлҝЙИЬРФБтЛбСОҙҰАн¶аУаөДBa2Ј«ЎЈјУИлҝЙИЬРФұөСОәуөД·ПЛ®ЦРBa2Ј«өДЕЁ¶ИУҰІ»РЎУЪ Ўш molЎӨLЈӯ1Ј¬И»әуФЩҪшРРәуРшҙҰАн·ҪДЬҙпөҪ№ъјТЕЕ·ЕұкЧјЎЈ
ўЪ»№Фӯ·ЁЈәCrO42Јӯ![]() Cr3Ј«
Cr3Ј«![]() Cr(OH)3ЎЈУГёГ·Ҫ·ЁҙҰАн10 m3 CrO42ЈӯөДОпЦКөДБҝЕЁ¶ИОӘ1.0ЎБ10ЎӘ3 molЎӨLЈӯ1өД·ПЛ®Ј¬ЦБЙЩРиТӘВМ·Ҝ(FeSO4ЎӨ7H2OЈ¬Па¶Ф·ЦЧУЦКБҝОӘ278) Ўш Kg(ұЈБфБҪО»РЎКэ)ЎЈ
Cr(OH)3ЎЈУГёГ·Ҫ·ЁҙҰАн10 m3 CrO42ЈӯөДОпЦКөДБҝЕЁ¶ИОӘ1.0ЎБ10ЎӘ3 molЎӨLЈӯ1өД·ПЛ®Ј¬ЦБЙЩРиТӘВМ·Ҝ(FeSO4ЎӨ7H2OЈ¬Па¶Ф·ЦЧУЦКБҝОӘ278) Ўш Kg(ұЈБфБҪО»РЎКэ)ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com