
题目列表(包括答案和解析)
下列叙述正确的是 ( )
A、这反应除了生成新的物质外,还伴随着能量的变化
B、物质燃烧一定是放热反应
C、放热的化学反应不需要加热就能发生
D、吸热反应不加热就不会发生
[ ]
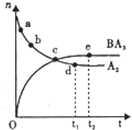 A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白:
A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白: CH3OH(g) △H1=-90.7 kJ . mol-1①
CH3OH(g) △H1=-90.7 kJ . mol-1①  CH3OCH3(g)+H2O(g) △H2 =-23.5 kJ . mol-1 ②
CH3OCH3(g)+H2O(g) △H2 =-23.5 kJ . mol-1 ②  CO2(g)+H2(g) △H3=-41.2 kJ . mol-1 ③
CO2(g)+H2(g) △H3=-41.2 kJ . mol-1 ③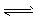 CH3OCH3(g)+CO2(g),则该反应的△H ___,平衡常数表达式为___,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会____(填升高、降低或不变)。
CH3OCH3(g)+CO2(g),则该反应的△H ___,平衡常数表达式为___,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会____(填升高、降低或不变)。 CH3OCH3(g)+3H2O(g) △H>0。 该反应在恒温、体积恒定的密闭容器中进行,下列不能作为该反应已达到化学平衡状态的判断依据的是____。
CH3OCH3(g)+3H2O(g) △H>0。 该反应在恒温、体积恒定的密闭容器中进行,下列不能作为该反应已达到化学平衡状态的判断依据的是____。 
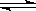 CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①
CH3OH(g) ΔH1=-90.7 kJ·mol-1 ①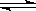 CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 ②
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 ②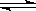 CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 ③
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 ③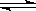 CH3OCH3(g)+CO2(g),则该反应的ΔH=__________,平衡常数表达式为____________________,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会________(填升高、降低或不变)。
CH3OCH3(g)+CO2(g),则该反应的ΔH=__________,平衡常数表达式为____________________,在恒温、可变容积的密闭容器中进行上述反应,增大压强,二甲醚的产率会________(填升高、降低或不变)。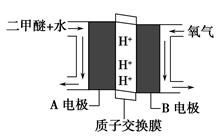
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com