
题目列表(包括答案和解析)
(1)三聚氰胺(结构如右图),由于其含氮量高被不法奶农添加到牛奶中
来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石。 
三聚氰胺中C原子的杂化形式是
二种环境的N原子的杂化形式分别是 , 。
(2)化合A是一种不稳定的物质,它的分子式可表示为OxFy,10mL A气体能分解成为15mL O2和10mL F2(同温同压)
①A的分子式是 ;
②已知A的分子中的x个氧原子呈…O-O-O…链状排列,则A的电子式是 ,A分子的结构式是 。
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++x R-H→Rx[CrCln(H2O)6-n]+xH+
交换出来的H+经测定,即可求出x和n,确定配离子的组成。
将含0.0015mol [CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol/L NaOH溶液25.00ml,推知:
x= ,n= , 该配离子的化学式为 。
(1)三聚氰胺(结构如右图),由于其含氮量高被不法奶农添加到牛奶中来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石。
三聚氰胺中C原子的杂化形式是
二种环境的N原子的杂化形式分别是 , 。
(2)化合A是一种不稳定的物质,它的分子式可表示为OxFy,10mL A气体能分解成为15mL O2和10mL F2(同温同压)
①A的分子式是 ;
②已知A的分子中的x个氧原子呈…O-O-O…链状排列,则A的电子式是 ,A分子的结构式是 。
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++x R-H→Rx[CrCln(H2O)6-n]+xH+
交换出来的H+经测定,即可求出x和n,确定配离子的组成。
将含0.0015mol[CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol/L NaOH溶液25.00ml,推知:
x= ,n= , 该配离子的化学式为 。
(1)三聚氰胺(结构如右图),由于其含氮量高被不法奶农添加到牛奶中 来“提高”蛋白质的含量,造成全国许多婴幼儿因食用这种奶粉而患肾结石。 
三聚氰胺中C原子的杂化形式是
二种环境的N原子的杂化形式分别是 , 。
(2)化合A是一种不稳定的物质,它的分子式可表示为OxFy,10mL A气体能分解成为15mL O2和10mL F2(同温同压)
①A的分子式是 ;
②已知A的分子中的x个氧原子呈…O-O-O…链状排列,则A的电子式是 ,A分子的结构式是 。
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++x R-H→Rx[CrCln(H2O)6-n]+xH+
交换出来的H+经测定,即可求出x和n,确定配离子的组成。
将含0.0015mol [CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol/L NaOH溶液25.00ml,推知:
x= ,n= , 该配离子的化学式为 。
已知A、B、C、D、E、F六种短周期元素的性质或结构信息如下表,请根据信息回答下列问题。
元素 性质或结构信息
A 单质常温下为固体,难溶于水易于溶CS2。能形成2种二元含氧酸。
B 原子的M层有1个未成对的p电子。核外p电子总数大于7。
C 单质曾被称为“银色的金子”。与锂形成的合金常用于航天飞行器。单质能溶强酸和强碱。
D 原子核外电子层上s电子总数比p电子总数少2个。单质和氧化物均为空间网状晶体,具有很高的熔、沸点。
E 其氧化物是汽车尾气的主要有害成分之一,也是空气质量预报的指标之一;该元素在三聚氰胺中含量较高。
F 周期表中电负性最大的元素
(1)A原子的最外层电子排布式 ,D原子共有 种不同运动状态的电子。
(2)F与E元素第一电离能的大小关系: > (填元素符号)。
(3)A,B两元素的氢化物分子中键能较小的是 ;分子较稳定的是 。(填分子式)
(4)C单质、镁、NaOH溶液可以构成原电池,则负极的电极反应式为_________________。
(5)F与钙可组成离子化合物,其晶胞结构如图所示,该化合物的电子式是 。已知该化合物晶胞1/8的体积为2.0×10-23cm3,求该离子化合物的密度,请列式并计算(结果保留一位小数):_______________________。

(15分)可以由下列反应合成三聚氰胺:CaO+3CCaC2+CO↑,CaC2+N2CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:______________________________________________________________________。
CaCN2中阴离子为CN,与CN互为等电子体的分子有N2O和________(填化学式),由此可以推知CN的空间构型为________。
(2)尿素分子中C原子采取________杂化。尿素分子的结构简式是________________。
(3)三聚氰胺  俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸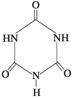 后,
后,
三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为______________。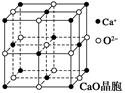
已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离 ________________ __(列出计算式)
CaO晶体和NaCl晶体的晶格能分别为:CaO 3 401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是______________ ______。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com