
题目列表(包括答案和解析)
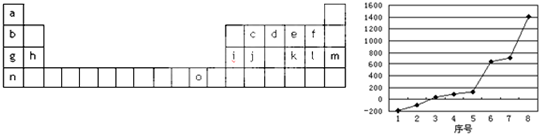
右图是周期表的一部分,已知A、B、C、D都是短周期元素,四种元素原子核外共有56个电子,推断A、B、C、D各是什么元素,写出他们的元素符号:A ,B ,C ,D 。
右图为周期表的一部分。已知A、B、C、D、E五种元素原子的核外共有85个电子,E原子核外有四个电子层,则B元素是

A. P B.S C.Cl D.Si
已知A、B、C、D、E、F六种元素的原子序数依次递增,都位于前四周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。F处于周期表中第9列。
(1)B、C、D三种元素的氢化物的沸点高低顺序为 ,稳定性顺序为 。
(2)同时含有A、B、D三种元素的化合物M是此类物质中为数不多的气体,且分子中所有原子共平面,则M中σ键和π键个数比为 ,B原子的杂化类型为 ,M能和水以任意比混溶的原因是 。
(3)C的最高价含氧酸根的空间构型为 ,E的基态原子的价电子排布式
为
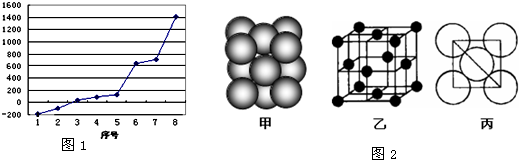
 (4)“生物金属”E内部原子的堆积方式与铜相同,都是面心立方堆积方式,如右图。则E晶胞中E的配位数为 ,若该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,E原子的摩尔质量为M g/mol,则E原子的半径为 cm
(4)“生物金属”E内部原子的堆积方式与铜相同,都是面心立方堆积方式,如右图。则E晶胞中E的配位数为 ,若该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,E原子的摩尔质量为M g/mol,则E原子的半径为 cm
(5)F可形成分子式均为F(NH3)5BrSO4的两种配合物,其中一种化学式为[F(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,产生的现象是 ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 。
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | ||||||||||||||||


| ||
| 8NAd3 |
| ||
| 8NAd3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com