
题目列表(包括答案和解析)
(9分)1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃ ,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2
,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2 - 二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:
- 二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白: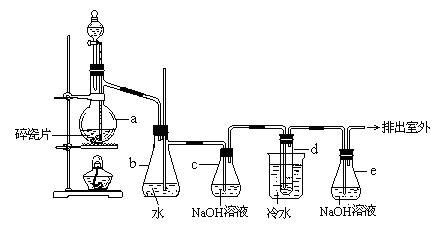
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式。
____________________________________________________________
____________________________________________________________
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管 d是否发生堵塞.请写出发生堵塞时瓶b中的现象。
d是否发生堵塞.请写出发生堵塞时瓶b中的现象。
_________________________________。
(3)容器c中NaOH溶液的作用是:__________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性 没有问题,试分析其可能的原因是:
没有问题,试分析其可能的原因是:
____________________________________________________________
(18分)镇痉药物C、化合物N以及高分子树脂 的合成路线如下:
的合成路线如下:
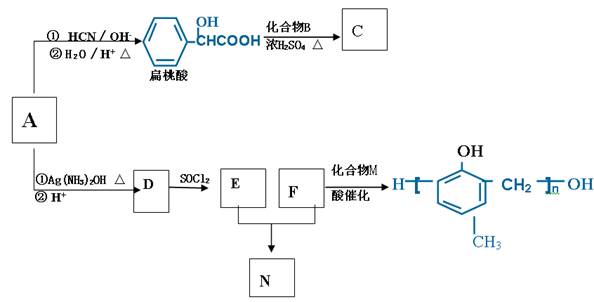
已知: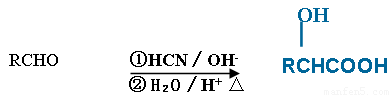
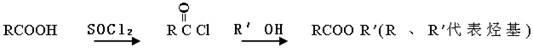
(1)A的含氧官能团的名称是 。
(2)A在催化剂作用下可与H2反应生成B。该反应的反应类型是 。
(3)酯类化合物C的分子式是C15H14O3,其结构简式是 。
(4)A发生银镜反应的化学方程式是 。
(5)扁桃酸(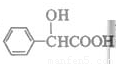 )有多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有 种,写出其中一种含亚甲基(―CH2―)的同分异构体的结构简式 。
)有多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有 种,写出其中一种含亚甲基(―CH2―)的同分异构体的结构简式 。
(6)F与M合成高分子树脂的化学方程式是 。
(7)N在NaOH溶液中发生水解反应的化学方程式是 。
(18分,每空3分)铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42—  2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是______ ______;电解液中H2SO4的浓度将变__ __;当外电路通过1 mol电子时,理论上负极板的质量增加___ ___g。
(2)电池使用一段时间后,若按图连接,则在A电极上生成___ __、B电极上生成__ __,此时铅蓄电池的正负极的极性将_ ___。(填“不变”或“对掉”)
(18分)下列为A、B、C、D四种物质的转化关系,a、b为反应条件,
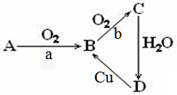
(1)若A为单质,a为点燃,b为催化剂、加热,
① D的化学式为
② 写出B到C的化学方程式 。
(2)若A为气态化合物,a为催化剂、加热,B到C转化不需要条件,
① A的化学式为 ,1mol A中含有的电子数为 NA (NA 为阿伏加德罗常数)。
② 写出C→D化学方程式 ,该反应中氧化剂与还原剂的质量之比为 。
?写出Cu与D溶液反应的离子方程式 。
(18分)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)地壳中含量居于第二位的元素在周期表中的位置是________________。
(2)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:
__________,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的离子化合物,写出其中一种化合物的电子式_______________。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,下列物质不能做该反应催化剂的是(填序号)________。
a.MnO2 b. CuSO4 c.Na2SO3 d.FeCl3
(5) W与④是相邻的同主族元素。在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式。
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3===3H3PO4+H2W↑ |
| 1 | | |
| 2 | | |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com