甲醛亦称“蚁醛”.含甲醛37~40%、甲醇8%的水溶液俗称“福尔马林”.甲醛是重要的有机合成原料,大量用于生产树脂、合成纤维、药物、涂料等.甲醛是世界卫生组织(WHO)确认的致癌物和致畸物质之一.我国规定:室内甲醛含量不得超过0.08mg?m
-3.
(1)下列说法或做法不合理的是
.(填字母)
a.用甲醛溶液浸泡水产品以长时间保持水产品的“新鲜”
b.刚装修的新房入住前房间内保持一定温度并注意通风
c.对人体健康有危害的吊白块的合成反应NaHSO
3+HCHO→NaO-CH
2-SO
3H的反应类型是加成反应
d.福尔马林可用于制作动物标本(或保存尸体)
(2)某研究性学习小组拟用甲醛法测定常见铵态氮肥的含氮量[资料:4NH
4++6HCHO=(CH
2)
6N
4H
++3H
++6H
2O,所生成的H
+和(CH
2)
6N
4H
+可用NaOH标准溶液滴定,采用酚酞作指示剂].用甲醛法测定含氮量,不适合的铵盐是
.(填字母)
a.NH
4HCO
3 b.(NH
4)
2SO
4 c.NH
4Cl
(3)甲醇脱氢是制甲醛最简单的工业方法:
反应Ⅰ:CH
3OH(g)→HCHO(g)+H
2(g);△H
1=92.09kJ?mol
-1,其平衡常数K
1=3.92×10
-11甲醇氧化是制甲醛的另一种工业方法,即甲醇蒸气和一定量的空气通过Ag催化剂层,甲醇即被氧化得到甲醛:
反应Ⅱ:CH
3OH(g)+
O
2(g)→HCHO(g)+H
2O(g);△H
2=-149.73kJ?mol
-1,其平衡常数K
2=4.35×10
29(上述数据均为298.15K下测定.)
①绿色化学提倡化工生产应提高原子利用率.原子利用率表示目标产物的质量与生成物总质量之比.反应
(填“Ⅰ”或“Ⅱ”)制甲醛原子利用率更高.从反应的焓变和平衡常数K值看,反应
(填“Ⅰ”或“Ⅱ”)制甲醛更加有利.
②反应Ⅱ自发进行的条件是
.
a.高温b.低温c.任何条件都自发
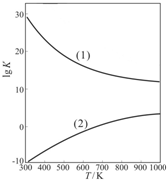
③右图是甲醇制甲醛有关反应的lgK(平衡常数的对数值)随温度T的变化.图中曲线(1)表示的是反应
(填“Ⅰ”或“Ⅱ”).

 )的反应中,原子利用率最高的是( )
)的反应中,原子利用率最高的是( )