(1)学生甲设想用图-1装置(A为电加热装置)从钛铁矿中提取氧。请写出FeTiO
3在加热时被H
2还原的化学方程式_________________________和最简便的实验步骤________(选填下列数字编号)。
①通入N
2;②停止通N
2;③通入H
2;④停止通H
2;⑤加热;⑥停止加热;⑦称取装置B的质量。
(2)学生乙设想用图-2装置(A为电加热装置)从钛铁矿中提取氧,并且认为该方案的意义在于:反应产生的CO
2可通过绿色植物的光合作用转化为营养物质,同时产生氧气:
6CO
2+6H
2O
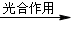
C
6H
12O
6(葡萄糖)+6O
2。实验过程中,称得反应前装置A中钛铁矿的质量为ag,炭粉的质量为bg,反应后装置B中产生CaCO
3的质量为cg,则钛铁矿中可提取氧的质量分数的表达式为________________。
(3)经专家评审后,认定两个方案都很有意义,但实验设计方面还存在不足之处,例如图-2装置在加热时,生成的CO
2不可能全部被澄清石灰水吸收,同时钛铁矿和炭粉在加热时还会产生CO,给实验带来误差。
①请对学生乙的设想提出改进措施:改用图-1装置,并在U型管B之前增加盛有________ 的燃烧管,________________。
②改进后,实验自始至终需持续向装置A中通入N
2的目的是________________。
[探究二]纳米TiO
2作为一种光催化剂越来越受到人们的关注,现正广泛开发运用。
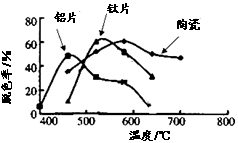
(4)某科研小组在不同的载体(钛片、铝片、陶瓷)表面制备二氧化钛薄膜,来考察不同载体TiO
2薄膜光催化使甲基橙脱色,每次光照20min取一次样,实验结果如图所示,下列说法正确的是________。




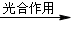 C6H12O6(葡萄糖)+6O2。实验过程中,称得反应前装置A中钛铁矿的质量为ag,炭粉的质量为bg,反应后装置B中产生CaCO3的质量为cg,则钛铁矿中可提取氧的质量分数的表达式为________________。
C6H12O6(葡萄糖)+6O2。实验过程中,称得反应前装置A中钛铁矿的质量为ag,炭粉的质量为bg,反应后装置B中产生CaCO3的质量为cg,则钛铁矿中可提取氧的质量分数的表达式为________________。