
题目列表(包括答案和解析)
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究性学习:
【查阅资料】金属活泼性不同,其硝酸盐分解产物不同
(1)K→Na活泼金属的硝酸盐分解生成亚硝酸盐和氧气;
(2)Mg→Cu等较活泼金属的硝酸盐分解生成氧化物、NO2和O2;
(3)Hg以后不活泼金属的硝酸盐分解生成金属、NO2和O2。
2KNO3![]() 2KNO2↑+O2↑ 2Cu(NO3)2
2KNO2↑+O2↑ 2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
2AgNO3![]() 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
【实验一】探究Fe(NO3)2热分解固体产物中Fe元素的价态。该小组甲同学将其溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
【提出猜想】
猜想一:Fe元素只显+2价;
猜想二:Fe元素只显______价;
猜想三:Fe元素_________。
【实验操作】①向一份溶液中滴入KSCN溶液;②稀酸性KMnO4溶液中滴入另一份溶液。
【实验现象】实验① ;
实验② 。
【实验结论】猜想二成立,则Fe(NO3)2分解的化学方程式是 。
 【实验二】探究Fe(NO3)2热分解气体产物的性质。小组乙、丙同学进行了如下图所示的实验(收集时操作恰当,几乎没有空气)
【实验二】探究Fe(NO3)2热分解气体产物的性质。小组乙、丙同学进行了如下图所示的实验(收集时操作恰当,几乎没有空气)
实验步骤:①连接仪器;②检查装置气密性;③取一定质量Fe(NO3)2装于大试管,并重新连接好仪器;④加热;⑤……
(1)乙同学使用A装置收集气体,恰好收集到27mL红棕色气体,要从水槽中取出量筒,乙同学的正确操作方法是
。
(2)乙同学用带火星木条检验量筒内气体时,发现木条燃烧,下列判断中正确的是 。
a.气体中只有NO2 b.气体是O2、NO2的混合物
c.支持燃烧的气体只有O2 d.NO2支持燃烧
现有实验药品:一定质量的锌(分片状和粒状两种)、浓H2SO4(密度1.84 g?cm-3)、水以及如右图所示装置。图中量气管B由甲、乙两根玻璃管组成,它们用橡皮管连通并装适量水。甲管有刻度(0~100 mL)。甲、乙两管可固定在铁架台上,供量气用。实验时乙管可上下移动,以调节液面高低。利用此装置可测定锌的相对原子质量(设锌全部反应,产生气体不超过50 mL)。回答下列问题:
(1)实验前应如何检查装置的气密性?  。
。
(2)①按图示装置实验,但保证不漏出H2,应如何操作?
。
②若改变气体发生装置,但仍要求保证不漏气,在中学的常用仪器中,应用(自选仪器) 仪器来装配;在检查了装置的气密性后,应如何操作: 。
(3)为了较准确地测量H2的体积,在读取反应前后甲管中液面的读数时,除注意视线与凹液面最低处相平外,还应注意 ,原因是 。
(4)设计一个不用量气管,而用中学化学中常用仪器测量H2体积的装置,应用的仪器(自选)是 。
| 沸点/℃ | 水溶性 |
甲醇 | 65 | 与水混溶 |
甲醛 | -21 | 与水混溶 |
图15-18是两个学生设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如(甲)和(乙)所示,试完成下列问题:?
?
图15-18
(1)若按(甲)装置进行实验,则通入A管的X是 ,B中反应的化学方程式为 。
(2)若按(乙)装置进行实验,则B管中应装 ,反应的化学方程式 。?
(3)C中应装的试剂是 。?
(4)在仪器组装完成后,加试剂前都必须要进行的操作是? ?,若添加药品后,如何检验乙装置的气密性? 。??
(5)两种装置中都需加热的仪器是 (填A、B、C),加热的方式分别为 ,实验完成时,都应先停止对? ?(填A、B、C)加热,再 。若实验完成时先打开D处气球的铁夹,再撤去酒精灯,打开铁夹的目的是? ?。简述工作原理 。
(6)你认为用哪套装置较好 (填“甲”或“乙”),理由是? 。?
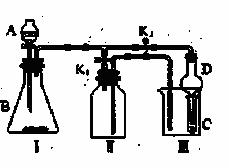
某化学兴趣小组设置了如图所示的实验装置,即可用于制取气体,又可用于验证物质的性质
(1)利用Ⅰ、Ⅱ装置制取气体(K2关闭、K1打开),甲同学认为:利用Ⅱ装置可以收集H2等气体,但不能收集O2 、NO2或NO气体,其理由是 。
(2)乙同学认为:利用Ⅱ装置作简单改进(但不改变瓶口朝向),
也可以收集O2、NO等气体,但不能收集NO2气体,其改进的方法
是 。
(3)丙同学想利用上述装置比较H2SO4、H2CO3和H2SiO3的酸性强弱(不必再选用其它酸性溶液,且通过一次实验就可以达到目的)。实验时,K1关闭、K2打开。锥形瓶内装 固体,装置C(试管)中所盛的试剂是 ;实验确认H2SO4、H2CO3和H2SiO3的酸性强弱出现的现象是
。
(4)丁同学想证明氧化性:Ca(ClO)2 >Cl2 > Br2,实验时,K1关闭、K2打开,则在A中加__________;B中加Ca(ClO)2,C中加________溶液,观察到C中的现象是__________________________;但是此装置在完成这个实验时尚存不足,其不足是_________________________。
用实验确定某酸HA是弱电解质.两同学的方案是:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质.
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是________.
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH________1(选填“>”、“<”或“=”).
乙方案中,说明HA是弱电解质的现象是________.
(a)装HCl溶液的试管中放出![]() 的速率快;
的速率快;
(b)装HA溶液的试管中放出![]() 的速率快;
的速率快;
(c)两个试管中产生气体速率一样快.
(3)请你评价:乙方案中难以实现之处和不妥之处__________________________、__________________________.
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com