
题目列表(包括答案和解析)
50ml0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,有两处缺点,其一是有处错误安装会导致热量散失较大,应该改正为 ,其二尚缺少一种玻璃仪器,这玻璃仪器名称是
(2)烧杯间填满碎纸条的作用是 。
(3)若大烧杯上不盖硬纸板,求得的反应热数值 (填“偏大”“偏小”或“无影响”)。
(4)实验中该用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
(填“偏大”、“偏小”或“无影响”)。
(6)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2-t1分别为![]() 2.2℃
2.2℃ ![]() 2.4℃
2.4℃ ![]() 3.4℃,则最终代入计算式的温差均值为 ℃
3.4℃,则最终代入计算式的温差均值为 ℃
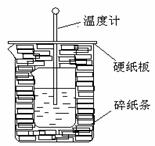
50ml0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在
如下图所示的装置中进行中和反应。通过测定反应过程
中放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)若大烧杯上不盖硬纸板,求得的中和热△H (填“偏大” “偏小”或“无影响”)。

(8分)50ml0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题: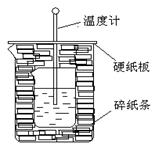
(1)从实验装置上看,有两处缺点,其一是有处错误安装会导致热量散失较大,应该改正为 ,其二尚缺少一种玻璃仪器,这玻璃仪器名称是
(2)烧杯间填满碎纸条的作用是 。
(3)若大烧杯上不盖硬纸板,求得的反应热数值 (填“偏大”“偏小”或“无影响”)。
(4)实验中该用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
(填“偏大”、“偏小”或“无影响”)。
(6)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2-t1分别为2.2℃ 2.4℃ 3.4℃,则最终代入计算式的温差均值为 ℃
(8分)50ml0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,有两处缺点,其一是有处错误安装会导致热量散失较大,应该改正为 ,其二尚缺少一种玻璃仪器,这玻璃仪器名称是
(2)烧杯间填满碎纸条的作用是 。
(3)若大烧杯上不盖硬纸板,求得的反应热数值 (填“偏大”“偏小”或“无影响”)。
(4)实验中该用60mL0.50mol·L-1盐酸跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
(填“偏大”、“偏小”或“无影响”)。
(6)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2-t1分别为2.2℃ 2.4℃ 3.4℃,则最终代入计算式的温差均值为 ℃

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com