
题目列表(包括答案和解析)
A.同时增大
B.同时减小
C.v1增大,v2减小
D.v1减小,v2增大
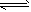 2CO(正反应吸热)反应速率为v1,N2+3H2
2CO(正反应吸热)反应速率为v1,N2+3H2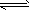 2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为 [ ]
A.同时增大 B.同时减小 C.v1增大,v2减小 D.vl减小,
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法研究反应速率的有关问题。
(1)实验1 探究Mg与盐酸反应速率的变化规律
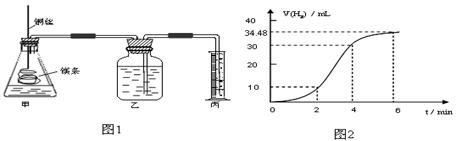
取一段镁条,用砂纸擦去表面的氧化膜,铜丝缠着镁条伸入装置甲中,使镁条浸入锥形瓶内的体积为2L稀盐酸(足量)中。镁条和盐酸反应生成H2的体积与反应时间的关系曲线如图2所示。
① 从图2中看出0-6min内平均反应速率最快的时间段是 。(填代号)
A.0-2min B.2-4min C.4-6min
② 请计算4-6min 时间内,用HCl表示的平均反应速率为________。(假设图2氢气体积均已换算为标准状况下的体积,且溶液体积变化可忽略)
③图1装置甲中与镁条相连的铜丝若一起浸入稀盐酸中对反应速率影响下列说法正确的是
A.加快反应速率但生成氢气的总量不变 B.减慢反应但增大生成氢气总量
C.不影响反应速率 D.加快反应速率但生成氢气的总量减小
(2)实验2 探究酸浓度对MnO2与H2O2反应速率的影响
已知MnO2+H2O2+2H+ Mn2++O2↑+2H2O,现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0 mL氧气所需时间。
|
实验编号 |
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
|
10%H2O2的体积/mL |
5.0 |
5.0 |
V1 |
V2 |
|
20%硫酸的体积/mL |
0 |
0.5 |
1.0 |
V3 |
|
水的体积/mL |
15 |
14.5 |
V4 |
13.5 |
|
所需时间t/s |
t1 |
t2 |
t3 |
t4 |
①上表中V1= mL, V3= mL。
②有同学提出实验I不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是 。
③若实验测得t2>t3>t4,则可得出的实验结论是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com