
题目列表(包括答案和解析)
 (2008?怀柔区二模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况用如图来表示.下列对该图象理解的叙述中,正确的是( )
(2008?怀柔区二模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相同的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况用如图来表示.下列对该图象理解的叙述中,正确的是( ) (2005?白下区一模)小红的外公家里有四种化肥,小红测试了四种化肥溶液的pH:尿素pH=7,碳酸氢铵pH=8,硫酸铵pH=5,氨水pH=11
(2005?白下区一模)小红的外公家里有四种化肥,小红测试了四种化肥溶液的pH:尿素pH=7,碳酸氢铵pH=8,硫酸铵pH=5,氨水pH=11| 小红探究的问题 | 小红的解答 |
| 这包化肥至少含有多少千克氮元素? | |
| 怎样鉴别它是碳酸氢铵而不是硫酸钾呢? | |
| 这包化肥是纯净物还是混合物? |
 (2005?白下区一模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如右图所示.下列对该图象理解的叙述中,正确的是( )
(2005?白下区一模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如右图所示.下列对该图象理解的叙述中,正确的是( )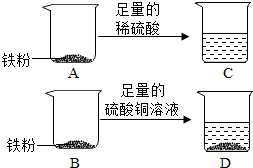 (2012?贵阳)实验室有一包纯净的铁粉,小明为了探究金属的化学性质并测定铁的相对原子质量,设计了如图的实验.
(2012?贵阳)实验室有一包纯净的铁粉,小明为了探究金属的化学性质并测定铁的相对原子质量,设计了如图的实验.| 2w |
| n-m |
| 2w |
| n-m |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com