
题目列表(包括答案和解析)
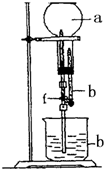 为探究NH3的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题:
为探究NH3的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题:(8分) (1)下列实验方法合理的是 (多选或错选不给分)
A、用加热法除去食盐固体中的氯化铵
B、将碘的饱和水溶液中的碘提取出来,可用酒精进行萃取
C、实验室制取Al(OH)3: 往AlCl3溶液中加入NaOH溶液至过量
D、往FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质
(2)SiO2广泛存在自然界中,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。写出工业上用石英制备粗硅的化学反应方程式
(3)铝是一种重要金属:铝与NaOH溶液反应的离子方程式为:
(4)将10.7g 氯化铵固体与足量消石灰混合加热使之充分反应。生成气体在标准状况下的体积是 L
(8分)(1)下列实验方法合理的是 (多选或错选不给分)
| A.用加热法除去食盐固体中的氯化铵 |
| B.将碘的饱和水溶液中的碘提取出来,可用酒精进行萃取 |
| C.实验室制取Al(OH)3: 往AlCl3溶液中加入NaOH溶液至过量 |
| D.往FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质 |
(8分) (1)下列实验方法合理的是 (多选或错选不给分)
A、用加热法除去食盐固体中的氯化铵
B、将碘的饱和水溶液中的碘提取出来,可用酒精进行萃取
C、实验室制取Al(OH)3: 往AlCl3溶液中加入NaOH溶液至过量
D、往FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质
(2)SiO2广泛存在自然界中,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。写出工业上用石英制备粗硅的化学反应方程式
(3)铝是一种重要金属:铝与NaOH溶液反应的离子方程式为:
(4)将10.7g 氯化铵固体与足量消石灰混合加热使之充分反应。生成气体在标准状况下的体积是 L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com