
题目列表(包括答案和解析)
某研究性学习小组设计用如下方法测定某居室空气中甲醛的含量(假设空气中无其他还原性气体):
Ⅰ.测定原理:KMnO4(H+)溶液为强氧化剂,可氧化甲醛和草酸,其反应的离子方程式为:
4![]() +5HCHO+12H+====4Mn2++5CO2↑+11H2O
+5HCHO+12H+====4Mn2++5CO2↑+11H2O
2![]() +5H2C2O4+6H+====2Mn2++10CO2↑+8H2O
+5H2C2O4+6H+====2Mn2++10CO2↑+8H2O
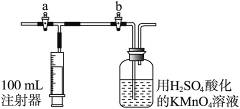
Ⅱ.测定装置:部分装置如下图所示(a、b为止水夹)
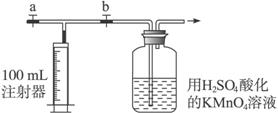
Ⅲ.实验步骤:
①检查装置气密性(气密性良好)。
②用A仪器准确移取25.00 mL 1.00×10-3 mol·L-1的高锰酸钾溶液(过量)于广口瓶中并滴入3滴6 mol·L-1 H2SO4溶液备用。
③将2.00×10-3 mol·L-1的草酸标准溶液置于A仪器中备用。
④打开a,关闭b,用注射器抽取100 mL新装修的室内空气。关闭a,打开b,再缓缓推动注射器,将气体全部推入高锰酸钾酸性溶液中,使其充分反应。再如此重复4次(共5次)。
⑤将广口瓶中的溶液转入锥形瓶中(润洗广口瓶2—3次,并将洗涤液全部转入锥形瓶)。
⑥用标准草酸溶液滴定锥形瓶中的溶液,记录滴定所消耗的草酸溶液体积。
⑦再重复实验2次。
Ⅳ.数据处理:分别于装修完工后的第1天、第7天、第30天(室内始终保持通风换气状况)对室内空气进行取样,通过实验测得以下三组数据(每次实验所取的KMnO4溶液均为25.00 mL):
装修后第n天 | 草酸溶液/mL | 甲醛的浓度/mg·m-3 | |||
1 | 2 | 3 | 平均值 | ||
1 | 15.86 | 15.72 | 15.67 | 15.75 |
|
7 | 26.24 | 26.36 | 26.31 | 26.30 |
|
30 | 30.90 | 30.67 | 30.81 | 30.79 |
|
请完成下列问题:
(1)A仪器名称是_________________ 。
(2)步骤④如果压送气体时速度过快,可能会产生什么不利后果?
_____________________________________________________________________。
(3)步骤⑤如果没有润洗,所测甲醛的含量将____________(填“偏高”“偏低”或“无影响”)。
(4)本实验是否需要指示剂(如果需要,请写出指示剂的名称;如果不需要,试说明终点时的实验现象):___________________________________________________________________。
(5)假设KMnO4溶液的物质的量浓度为c1 mol·L-1,所取KMnO4溶液的体积为V1 mL;草酸溶液的物质的量浓度为c2 mol·L-1,消耗草酸溶液的平均体积为V2 mL。
则:计算室内空气中甲醛浓度(mg·m-3)的代数式为____________,第30天室内空气中甲醛浓度为____________,并判断此时主人____________(填“能”或“否”)入住。
常温下甲醛是一种无色、有特殊刺激性气味的气体,易溶于水,是世界卫生组织(WHO)确定的致癌物和致畸形物之一。我国规定:居室空气中甲醛的最高容许浓度为0.08 mg/m3。
某研究性学习小组设计用如下方法测定某居室空气中甲醛的含量(假设空气中无其他还原性气体):
(1)测定原理:KMnO4(H+)溶液为强氧化剂,可氧化甲醛和草酸。
反应的离子方程式为:![]()
![]()
(2)测定装置:部分装置如右图所示(a、b为止水夹)。
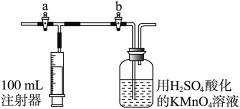
(3)实验步骤:
①检查装置气密性(气密性良好)。
②用__________(填仪器名称)准确移取25.00 mL 1.00×10-3 mol·L-1 的高锰酸钾溶液(过量)于广口瓶中并滴入3滴6 mol·L-1 H2SO4溶液备用。
③将2.00×10-3 mol·L-1的草酸标准溶液置于__________(填仪器名称)中备用。
④打开a,关闭b,用注射器抽取100 mL新装修的室内空气。关闭a,打开b,再缓缓推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应。再如此重复4次(共5次)。如果压送气体时速度过快,可能会产生什么不利后果?______________________________。
⑤将广口瓶中的溶液转入锥形瓶中(润洗广口瓶2~3次,并将洗涤液全部转入锥形瓶)。如果没有润洗,所测甲醛的含量将__________(填“偏高”“偏低”或“无影响”)。
⑥用草酸标准溶液滴定锥形瓶中的溶液,并记录滴定所消耗的草酸溶液体积。
本实验是否需要指示剂?(如果需要,请写出指示剂的名称;如果不需要,试说明终点时的实验现象)______________________________。
⑦再重复实验两次。
(4)数据处理:分别于装修完工后的第1天、第7天、第30天(室内始终保持通风换气状况)对室内空气进行取样,通过实验测得以下三组数据(每次实验所取的KMnO4溶液均为25.00 mL):
| 装置后 第n天 | 草酸溶液/mL | 甲醛的浓度mg/m3 | |||
| 1 | 2 | 3 | 平均值 | ||
| 1 | 15.86 | 15.72 | 15.67 | 15.75 | |
| 7 | 26.17 | 26.36 | 26.38 | 26.30 | |
| 30 | 30.90 | 30.67 | 30.81 | 30.79 | |
设KMnO4溶液的物质的量浓度为c1 mol·L-1,KMnO4溶液的体积为V1 mL;草酸溶液的物质的量浓度为c2 mol·L-1,草酸溶液的平均体积为V2 mL。
则:室内空气中甲醛浓度(mg/m3)的代数式为__________,第30天室内空气中甲醛浓度为__________(精确到小数点后两位),并判断此时主人__________(填“能”或“不能”)入住。
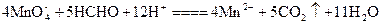
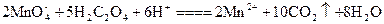
| 装置后 第n天 | 草酸溶液/mL | 甲醛的浓度mg/m3 | |||
| 1 | 2 | 3 | 平均值 | ||
| 1 | 15.86 | 15.72 | 15.67 | 15.75 | |
| 7 | 26.17 | 26.36 | 26.38 | 26.30 | |
| 30 | 30.90 | 30.67 | 30.81 | 30.79 | |
实验室里研究不同价态硫元素间的转化
1.二氧化硫(SO2)
(1)物理性质:通常情况下,二氧化硫________色,有________气味,比空气________,有________性,________溶于水.标准状况下,1体积水能溶解________体积二氧化硫.
(2)化学性质:二氧化硫中硫元素为+4价(中间价态),所以二氧化硫既有________又有________,二氧化硫是酸性氧化物,是________的酸酐.
①氧化性:SO2+2H2S![]() ________
________
②还原性:2SO2+O2![]() ________
________
SO2+Cl2+2H2O![]() ________
________
③酸性氧化物:与H2O、NaOH、Ca(OH)2等物质反应.
SO2+H2O![]() ________
________
④漂白性
可以使品红或其他有色物质褪色.原理是:二氧化硫能与某些有色物质化合生成不稳定的无色物质.这种无色物质受热或光照时易分解,放出SO2,恢复原来的颜色.
2.硫酸(H2SO4)
(1)物理性质:纯硫酸是________色、黏稠、________状液体,沸点________、难挥发.常用的浓硫酸质量分数是________,密度比水________.硫酸溶于水时放出大量的热.
②脱水性
浓硫酸能从一些有机物中将氢、氧两元素按H2O的组成(H∶O=2∶1)脱去.
例如:浓硫酸能使火柴棒、纸张变黑,就体现了其脱水性.
③强氧化性
Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
2H2SO4(浓)+C![]() ________.
________.
常温下,冷的浓H2SO4能使Fe和Al的表面形成一层________保护膜,阻止了内部金属与H2SO4反应.这种现象叫钝化.
总结:不同价态硫元素间的相互转化
0→-2:Fe+S![]() FeS,H2+S
FeS,H2+S![]() H2S……
H2S……
0→+4:S+O2![]() SO2,S+2H2SO4(浓)
SO2,S+2H2SO4(浓)![]() 3SO2↑+2H2O
3SO2↑+2H2O
0→+6:S+6HNO3(浓)![]() H2SO4+6NO2↑+2H2O
H2SO4+6NO2↑+2H2O
-20:2H2S+SO2![]() 2H2O+3S↓,H2S+Cl2
2H2O+3S↓,H2S+Cl2![]() 2HCl+S↓……
2HCl+S↓……
-2→+4:H2S+3H2SO4(浓)![]() 4SO2+4H2O
4SO2+4H2O
-2→+6:H2S+8HNO3(浓)![]() H2SO4+8NO2+4H2O
H2SO4+8NO2+4H2O
+4→0:2H2S+SO2![]() 2H2O+3S↓
2H2O+3S↓
+4→+6:2SO2+O2![]() ________……
________……
+6→+4:Cu+2H2SO4(浓)![]() ________
________
理化性质:
又名亚硫酸酐(1),无色有强烈辛辣刺激味的不燃性气体。相对分子质量64.07,密度
职业接触:
燃烧含硫燃料(3)、熔炼硫化矿石、烧制硫磺、制造硫酸和亚硫酸、硫化橡胶、制冷(4)、漂白(5)、消毒(6)、熏蒸杀虫、镁冶炼、石油精炼、某些有机合成等作业工人和有关人员皆有可能接触。另外,它是常见的工业废气及大气污染的成分(7)。
毒性:
属中等毒类,对眼和呼吸道有强烈刺激作用(8),吸入高浓度二氧化硫可引起喉水肿、肺水肿、声带水肿及痉挛导致窒息。
根据以上文字内容完成(1)—(7)小题。
(1)亚硫酐是亚硫酸酸酐的简称。无机酸的酸酐是一种氧化物,其中非氧元素在氧化物中的化合价与该元素在酸中的化合价相同。据此判断下列各组合不是酸酐及其对应的酸的是( )
A.SO3 H2SO4 B.CO2 H2CO
(2)文中(2)处所述的反应的化学方程式为_______________________________ ;这两个反应的反应类型可描述为_________________。
A.化合反应 化合反应 B.化合反应 氧化还原反应
C.氧化还原反应 化合反应 D.氧化还原反应 氧化还原反应
(3)含硫燃料主要指( )
A.天然气 B.煤 C.石油 D.硫化氢气体
(4)二氧化硫用于制冷主要是因为二氧化硫( )
A.易被氧化 B.易溶于水 C.易液化 D.有毒
(5)下列物质能用二氧化硫漂白的是( )
A.石蕊溶液 B.溴水 C.品红溶液 D.酸性KMnO4溶液
(6)2003年春天我国人民团结奋斗,取得了抗击“非典型肺炎”的胜利。抗非过程中最重要的措施就是消毒。下列物质可以用于环境消毒的是( )
A.二氧化氯 B.过氧乙酸 C.“
(7)下列气体中不属于大气污染物的是( )
A.氯气 B.二氧化碳 C.二氧化硫 D.二氧化氮
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com