
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
ЎЈ јЧЎўТТБҪёцСРҫҝРЎЧйЈ¬УГТФПВБҪЦЦ·Ҫ·ЁУЙCu·ЫЦЖCu(NO3)2ИЬТәЎЈ
(1)јЧЧйУГa g Cu·ЫЈ¬ФЪјУИИМхјюПВЈ¬УлҝХЖшід·Ц·ҙУҰЈ¬И»әуҪ«ЙъіЙөДCuOИ«ІҝИЬУЪККБҝөДПЎHNO3ИЬТәЦРЈ¬ЦЖөГCu(NO3)2ИЬТәЎЈФтПыәДөДO2өДОпЦКөДБҝКЗ Ј¬
ПыәДөДHNO3өДОпЦКөДБҝКЗ
(2)ТТЧйУГa g Cu·ЫИ«ІҝИЬУЪТ»¶ЁБҝөДЕЁHNO3ЦРЈ¬ІвөГЙъіЙөДЖшМеФЪұкЧјЧҙҝцПВМе»эОӘb L
(І»ҝјВЗNO2ЧӘ»ҜіЙN2O4)ЎЈФтПыәДөДHNO3өДОпЦКөДБҝКЗ molЎЈ
ОӘПыіэОЫИҫЈ¬Ҫ«ЙъіЙөДЖшМеНЁИлЛ®ЦРІўН¬КұНЁИлO2Ј¬К№ЙъіЙөДЖшМеНкИ«ИЬУЪЛ®Ј¬ФтПыәДO2өДОпЦКөДБҝКЗ molЈ»ИфҪ«ЙъіЙөДЖшМеНЁИлNaOHИЬТәЦРЈ¬ЖшМеұ»НкИ«ОьКХЈ¬ІъОпЦ»УРNaNO3ЎўNaNO2әНH2OЈ¬ФтЙъіЙNaNO2өДОпЦКөДБҝКЗ molЎЈ
ўсЎЈТ»¶ЁОпЦКөДБҝЕЁ¶ИИЬТәөДЕдЦЖәНЛбјоЦРәНөО¶ЁКЗЦРС§»ҜС§ЦРБҪёцөдРНөД¶ЁБҝКөСйЎЈДіСРҫҝРФС§П°РЎЧйФЪКөСйКТЦРЕдЦЖ1mol/LөДПЎБтЛбұкЧјИЬТәЈ¬И»әуУГЖдөО¶ЁДіОҙЦӘЕЁ¶ИөДNaOHИЬТәЎЈПВБРУР№ШЛө·ЁЦРХэИ·өДКЗ______________ЈЁҙр°ёҝЙДЬІ»ОЁТ»Ј©
AЎўКөСйЦРЛщУГөҪөДөО¶Ё№ЬЎўИЭБҝЖҝЈ¬ФЪК№УГЗ°ҫщРиТӘјмВ©Ј»
BЎўИз№ыКөСйЦРРиУГ60mL өДПЎБтЛбұкЧјИЬТәЈ¬ЕдЦЖКұУҰСЎУГ100mLИЭБҝЖҝЈ»
CЎўИЭБҝЖҝЦРә¬УРЙЩБҝХфБуЛ®Ј¬»бөјЦВЛщЕдұкЧјИЬТәөДЕЁ¶ИЖ«РЎЈ»
DЎўЛбКҪөО¶Ё№ЬУГХфБуЛ®ПҙөУәуЈ¬јҙЧ°ИлұкЧјЕЁ¶ИөДПЎБтЛбЈ¬ФтІвөГөДNaOHИЬТәөДЕЁ¶ИҪ«Ж«ҙуЈ»
EЎўУГјЧ»щіИЧчЦёКҫјБЈ¬өО¶ЁЦХөгКұЈ¬ИЬТәСХЙ«ҙУіИЙ«ұдОӘәмЙ«Ј»
FЎўЕдЦЖИЬТәәНЦРәНөО¶ЁөДБҪёцКөСйЦРЈ¬ИфФЪЧоәуТ»ҙО¶БКэҫщё©КУ¶БКэЈ¬ФтөјЦВКөСйҪб№ы¶јЖ«ҙуЎЈ
ўт . ПЦУГИзНјЛщКҫөДЧ°ЦГЦЖИЎҪП¶аБҝөДұҘәНВИЛ®ІўІв¶ЁұҘәНВИЛ®өДpHЎЈ
»ШҙрУР№ШОКМвЈә
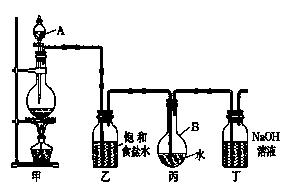
ЈЁ1Ј©РҙіцУР№Ш»ҜС§·ҪіМКҪЎЈ
Ч°ЦГјЧЈә____________________________________ Ј»
Ч°ЦГ¶ЎЈә __________________ ЎЈ
ЈЁ2Ј©ЦӨГчВИЛ®ТСұҘәНөДПЦПуКЗ ЎЈ
ЈЁ3Ј©ЦЖИЎҪбКшКұЈ¬Ч°ЦГұыөДТәМеЦРә¬УРөДОўБЈКЗ ЈЁУГОўБЈ·ыәЕұнКҫ Ј©Ј»
(4)Ифі·ИҘЧ°ЦГТТЈ¬ЦұҪУҪ«Ч°ЦГјЧәНұыПаБ¬ЎЈХвСщЧц¶ФКөСйІв¶ЁҪб№ыөДУ°ПмКЗЈә ЎЈ
Ів¶ЁұҘәНВИЛ®өДpH·Ҫ·ЁКЗ_______________________________________________ЎЈ
ўу.КөСйЙијЖЈәЦӨГчNaOH№ММеФЪҝХЖшЦР·ЕЦГІҝ·ЦұдЦК
_______________________________________________________________
_______________________________________________________________________
ўсЎЈТ»¶ЁОпЦКөДБҝЕЁ¶ИИЬТәөДЕдЦЖәНЛбјоЦРәНөО¶ЁКЗЦРС§»ҜС§ЦРБҪёцөдРНөД¶ЁБҝКөСйЎЈДіСРҫҝРФС§П°РЎЧйФЪКөСйКТЦРЕдЦЖ1mol/LөДПЎБтЛбұкЧјИЬТәЈ¬И»әуУГЖдөО¶ЁДіОҙЦӘЕЁ¶ИөДNaOHИЬТәЎЈПВБРУР№ШЛө·ЁЦРХэИ·өДКЗ______________ЈЁҙр°ёҝЙДЬІ»ОЁТ»Ј©
AЎўКөСйЦРЛщУГөҪөДөО¶Ё№ЬЎўИЭБҝЖҝЈ¬ФЪК№УГЗ°ҫщРиТӘјмВ©Ј»
BЎўИз№ыКөСйЦРРиУГ60mL өДПЎБтЛбұкЧјИЬТәЈ¬ЕдЦЖКұУҰСЎУГ100mLИЭБҝЖҝЈ»
CЎўИЭБҝЖҝЦРә¬УРЙЩБҝХфБуЛ®Ј¬»бөјЦВЛщЕдұкЧјИЬТәөДЕЁ¶ИЖ«РЎЈ»
DЎўЛбКҪөО¶Ё№ЬУГХфБуЛ®ПҙөУәуЈ¬јҙЧ°ИлұкЧјЕЁ¶ИөДПЎБтЛбЈ¬ФтІвөГөДNaOHИЬТәөДЕЁ¶ИҪ«Ж«ҙуЈ»
EЎўУГјЧ»щіИЧчЦёКҫјБЈ¬өО¶ЁЦХөгКұЈ¬ИЬТәСХЙ«ҙУіИЙ«ұдОӘәмЙ«Ј»
FЎўЕдЦЖИЬТәәНЦРәНөО¶ЁөДБҪёцКөСйЦРЈ¬ИфФЪЧоәуТ»ҙО¶БКэҫщё©КУ¶БКэЈ¬ФтөјЦВКөСйҪб№ы¶јЖ«ҙуЎЈ
ўт . ПЦУГИзНјЛщКҫөДЧ°ЦГЦЖИЎҪП¶аБҝөДұҘәНВИЛ®ІўІв¶ЁұҘәНВИЛ®өДpHЎЈ
»ШҙрУР№ШОКМвЈә
ЈЁ1Ј©РҙіцУР№Ш»ҜС§·ҪіМКҪЎЈ
Ч°ЦГјЧЈә____________________________________Ј»
Ч°ЦГ¶ЎЈә __________________ ЎЈ
ЈЁ2Ј©ЦӨГчВИЛ®ТСұҘәНөДПЦПуКЗ ЎЈ
ЈЁ3Ј©ЦЖИЎҪбКшКұЈ¬Ч°ЦГұыөДТәМеЦРә¬УРөДОўБЈКЗ ЈЁУГОўБЈ·ыәЕұнКҫЈ©Ј»
(4)Ифі·ИҘЧ°ЦГТТЈ¬ЦұҪУҪ«Ч°ЦГјЧәНұыПаБ¬ЎЈХвСщЧц¶ФКөСйІв¶ЁҪб№ыөДУ°ПмКЗЈә ЎЈ
Ів¶ЁұҘәНВИЛ®өДpH·Ҫ·ЁКЗ_______________________________________________ЎЈ
ўу.КөСйЙијЖЈәЦӨГчNaOH№ММеФЪҝХЖшЦР·ЕЦГІҝ·ЦұдЦК
_______________________________________________________________
_______________________________________________________________________
ЈЁ5·ЦЈ©Ј¬ЈЁ1Ј©ТФјЧНйОӘИјБПЦЖЧчРВРНИјБПөзіШЈ¬өзҪвЦКОӘЗвСх»ҜјШИЬТәЎЈөзіШёә·ҙУҰКҪОӘ Ј»·ЕөзКұјШАлЧУТЖПтөзіШөД ЈЁМоЎ°ХэЎұ»тЎ°ёәЎұЈ© ј«
ЈЁ2Ј©МјЗв»ҜәПОпНкИ«ИјЙХЙъіЙCO2әНH2OЎЈіЈОВіЈС№ПВЈ¬ҝХЖшЦРөДCO2ИЬУЪЛ®Ј¬ҙпөҪЖҪәвКұЈ¬ИЬТәpH=5.60Ј¬c(H2CO3)=1.5ЎБ10-5molЎӨL-1ЎЈИфәцВФЛ®өДөзАлј°H2CO3өДөЪ¶юј¶өзАлЈ¬
ФтH2CO3 HCO3-Ј«H+өДЖҪәвіЈКэK1= ЈЁТСЦӘ10-5.60=2.5ЎБ10-6Ј©
ЈЁ3Ј©іЈОВПВЈ¬0.1 molЎӨL-1NaHCO3ИЬТәөДpHҙуУЪ8Ј¬ФтИЬТәЦР
c(H2CO3) c(CO32-)ЈЁМоЎ°ЈҫЎұЎўЎ°=Ўұ»тЎ°ЈјЎұЈ©Ј¬ФӯТтКЗ
ЈЁУГАлЧУ·ҪіМКҪәНұШТӘөДОДЧЦЛөГчЈ©ЎЈ
ЈЁ5·ЦЈ©Ј¬ЈЁ1Ј©ТФјЧНйОӘИјБПЦЖЧчРВРНИјБПөзіШЈ¬өзҪвЦКОӘЗвСх»ҜјШИЬТәЎЈөзіШёә·ҙУҰКҪОӘ Ј»·ЕөзКұјШАлЧУТЖПтөзіШөД ЈЁМоЎ°ХэЎұ»тЎ°ёәЎұЈ© ј«
ЈЁ2Ј©МјЗв»ҜәПОпНкИ«ИјЙХЙъіЙCO2әНH2OЎЈіЈОВіЈС№ПВЈ¬ҝХЖшЦРөДCO2ИЬУЪЛ®Ј¬ҙпөҪЖҪәвКұЈ¬ИЬТәpH=5.60Ј¬c(H2CO3)=1.5ЎБ10-5 molЎӨL-1ЎЈИфәцВФЛ®өДөзАлј°H2CO3өДөЪ¶юј¶өзАлЈ¬
ФтH2CO3  HCO3-Ј«H+өДЖҪәвіЈКэK1= ЈЁТСЦӘ10-5.60=2.5ЎБ10-6Ј©
HCO3-Ј«H+өДЖҪәвіЈКэK1= ЈЁТСЦӘ10-5.60=2.5ЎБ10-6Ј©
ЈЁ3Ј©іЈОВПВЈ¬0.1 molЎӨL-1NaHCO3ИЬТәөДpHҙуУЪ8Ј¬ФтИЬТәЦР
c(H2CO3) c(CO32-)ЈЁМоЎ°ЈҫЎұЎўЎ°=Ўұ»тЎ°ЈјЎұЈ©Ј¬ФӯТтКЗ
ЈЁУГАлЧУ·ҪіМКҪәНұШТӘөДОДЧЦЛөГчЈ©ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com