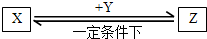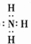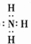X、Y、Z、W是原子序数依次增大的四种短周期元素,且四种元素的原子序数之和为32.其中X是元素周期表中原子半径最小的元素,Y、Z左右相邻,Z、W位于同一主族.
请回答下列问题:
(1)X是
H
H
(填元素符号).
(2)X与Y组成的最简单化合物的电子式为
.
(3)由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与金属铜反应,该反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.
(4)由X、Y、Z、W四种元素组成一种离子化合物A.
①已知在加热条件下1mol A能与足量的NaOH溶液反应生成标准状况下44.8L气体.写出在加热条件下A与NaOH溶液反应的离子方程式:
H2O+SO32-+Cl2=2Cl-+SO42-+2H+
H2O+SO32-+Cl2=2Cl-+SO42-+2H+
.
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式:
H2O+SO32-+Cl2=2Cl-+SO42-+2H+
H2O+SO32-+Cl2=2Cl-+SO42-+2H+
.
(5)由X、Y、Z、W和Fe五种元素可组成相对分子质量为392的化合物B,已知1mol B中含有6mol结晶水.现对化合物B进行如下实验:
a.向B的溶液中加入过量浓NaOH溶液并加热,产生白色沉淀和无色有刺激性气味的气体,白色沉淀迅速变为灰绿色,最终变为红褐色.
b.另取少量B的溶液,向其中加入过量BaCl
2溶液时产生白色沉淀,再加入稀盐酸沉淀不溶解.
由上述实验可推出B的化学式为
(NH4)2Fe(SO4)2?6H2O
(NH4)2Fe(SO4)2?6H2O
.