
题目列表(包括答案和解析)
(10分)某有机物A,在不同条件下反应分别生成B1和C1,B2和C2;而B1和C1在一定条件下又能分别转化为B2和C2,C2能进一步氧化,反应如下:
 又知:Bl能使溴水褪色,又可与碳酸钠溶液反应放出CO2。试回答:
又知:Bl能使溴水褪色,又可与碳酸钠溶液反应放出CO2。试回答:
(1)B2属于 ,
C1属于
(填写序号)
A.溴代饱和一元醇
B. 溴代不饱和一元醇
C.饱和一元醇
D.不饱和一元醇
E.溴代饱和羧酸盐 F. 溴代不饱和羧酸盐 G. 饱和羧酸盐 H.不饱和羧酸盐
(2)写出A、B1、C2的结构简式:
A B1 C2 。
(3)写出下列反应的化学方程式:
①a→b .
②C1→C2
。
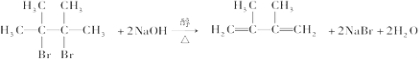
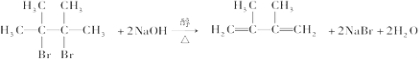
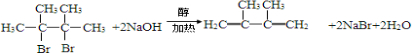

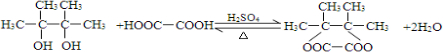
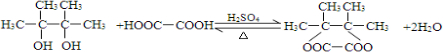
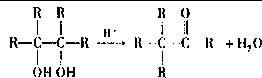 (-R为烃基),请写出E在酸性条件下生成G的化学反应方程式:
(-R为烃基),请写出E在酸性条件下生成G的化学反应方程式: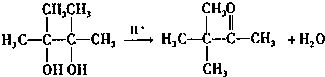
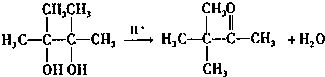
(10分)某研究性学习小组用电解 溶液的方法测定铜的相对原子质量(装置如图),实验中测得某电极的质量增重为m g,已知氧元素相对原子质量为16。请回答:
溶液的方法测定铜的相对原子质量(装置如图),实验中测得某电极的质量增重为m g,已知氧元素相对原子质量为16。请回答: 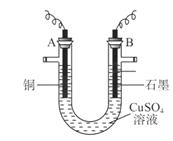
(1)m g应为 极的质量增重(填A或B),电解总反应的离子方程式为 ;
(2)本实验(电解 溶液)中,学习小组采用两套方案测定铜的相对原子质量。
溶液)中,学习小组采用两套方案测定铜的相对原子质量。
①第一套方案中,同学们测得气体的体积为V L(标准状况),则铜的相对原子质量是(用m、V表示) ;
②第二套方案中,以下数据需要测定的是(填序号) 。
a. A极增加的质量 b. 整套装置减少的质量
c. 电解后溶液的体积 d. 电解后溶液的pH(可由此计算出溶液中H+的物质的量浓度)
(10分)
某实验需要100 mL、0.1 mol/L的Na2CO3溶液,现通过如下操作配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用 (填仪器名称)搅拌
②把①所得溶液冷却到室温后,小心转入 (填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用 (填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是 (填序号)。
(2)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为 。
(3)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.01" mol/L的溶液,则稀释后溶液的体积为 mL
(4)在配制100 mL、0.1 mol/L的Na2CO3溶液时,下列操作中的 会导致结果偏低(请用
序号填写)
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.定容时俯视刻度线
c.定容时仰视刻度线
d.干净的容量瓶未经干燥就用于配制溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com