
题目列表(包括答案和解析)
要同时测定混有少量氯化钠杂质的芒硝(Na2SO4·nH2O)的纯度和结晶水含量,按下面流程进行实验。
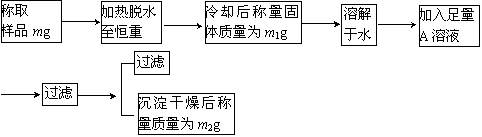
试回答:
(1)加热脱水时,若有固体飞溅出来造成损失,则会使测得的结晶水的含量偏________。加热脱水后,若将样品露置于空气中冷却,则会使测得的结晶水含量偏________。
(2)现有AgNO3、BaCl2、CaCl2、Ba(NO3)2、Ba(OH)2五种溶液,从测定的准确性考虑,可作为A溶液的是________;若加入A溶液的量不足,会使测得的纯度偏________;判断A溶液是否足量的方法是________。
(3)过滤时,应把滤纸上的沉淀洗涤干净,洗涤沉淀的方法是________,若不洗涤,则会使测得的纯度偏________。
(4)通过实验,测得芒硝的化学式中的n值为10,则芒硝的纯度为________%。
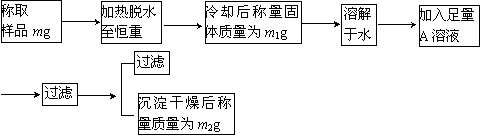
试回答:
(1)加热脱水时,若有固体飞溅出来造成损失,则会使测得的结晶水的含量偏________。加热脱水后,若将样品露置于空气中冷却,则会使测得的结晶水含量偏________。
(2)现有AgNO3、BaCl2、CaCl2、Ba(NO3)2、Ba(OH)2五种溶液,从测定的准确性考虑,可作为A溶液的是________;若加入A溶液的量不足,会使测得的纯度偏________;判断A溶液是否足量的方法是________。
(3)过滤时,应把滤纸上的沉淀洗涤干净,洗涤沉淀的方法是________,若不洗涤,则会使测得的纯度偏________。
(4)通过实验,测得芒硝的化学式中的n值为10,则芒硝的纯度为________%。
31 |
30 |
| 2 |
| 3 |
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 无明显现象 |
| ② | B+D | 有无色无味气体放出 |
| ③ | C+B | 有白色沉淀生成 |
| ④ | A+D | 有白色沉淀生成 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com