
题目列表(包括答案和解析)
|
下列仪器中,能用于直接加热的是 | |
| [ ] | |
A. |
量筒 |
B. |
容量瓶 |
C. |
蒸发皿 |
D. |
蒸馏烧瓶 |
(创新题)(1)下列物质中属于电解质的是________.能溶于水并且能够完全电离的是________,请写出其电离方程式.
①NaCl ②CO2 ③C2H5OH ④Ca(OH)2 ⑤BaSO4 ⑥Fe ⑦蔗糖
(2)用下列仪器的编号回答问题:
①容量瓶 ②蒸馏烧瓶 ③酸式滴定管 ④量筒 ⑤烧杯 ⑥托盘天平 ⑦分液漏斗
a.加热时必须垫石棉网的有________,b.使用时必须检查是否漏水的有________,c.标有零刻度的有________.

(1)以下各种尾气吸收装置中,适合于吸收HCl气体,而且能防止倒吸的有________
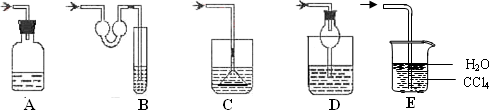
(2)对下列仪器回答下列问题:
A、容量瓶 B、蒸馏烧瓶 C、滴定管 D、量筒 E、烧杯
F、蒸发皿 G、分液漏斗
①标有“0”刻度的有________(填序号);
②使用时必须检查是否漏水的有________(填序号);
③对允许加热的仪器,加热时必须垫上石棉网的有________(填序号);
(3)用固体NaOH配制250mL0.5mol·L-1NaOH溶液,下列操作使所配制的NaOH溶液浓度偏高的有:________(填写代号,每选对一个得1分,选错倒扣分)
①称取固体NaOH时未用小烧杯
②没有用水冲洗烧杯2~3次
③定容时,俯视液面使与刻度相切
④溶液配好摇匀后,发现液面低于刻度线,又加水至液面与刻度相切
⑤将未冷却的溶液注入容量瓶后,马上定容
⑥样品中混有Na2O杂质

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com