
题目列表(包括答案和解析)
 (1)原电池反应通常是放热反应,下列化学反应在理论上可设计成原电池是
(1)原电池反应通常是放热反应,下列化学反应在理论上可设计成原电池是
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |

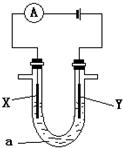
(1)X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中总反应的离子方程式为_______________,在X极附近观察到的实验现象是_______________。检验Y电极反应产物的方法是_______________。
(2)若想用电解实验制得白色纯净的Fe(OH)2沉淀,a仍是饱和NaCl溶液,则Y电极反应式为 _______________,往U型管添加完饱和NaCl溶液后需加入少量苯,苯的作用是_______________。
(3)若想用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是_______________,Y电极反应式为___________________。
电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
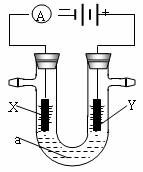
(1)X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中总反应的离子方程式为 ,在X极附近观察到的实验现象是 。检验Y电极反应产物的方法是 。
(2)若想用电解实验制得白色纯净的Fe(OH)2沉淀,a仍是饱和NaCl溶液,则Y电极反应式为 ,往U型管添加完饱和NaCl溶液后需加入少量苯,苯的作用是 。
(3)若想用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是
, Y电极反应式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com