
题目列表(包括答案和解析)
(14分)我国化学家侯德榜根据NaHCO3的溶解度比NaCl、Na2CO3、NH4C1都小的性质,运用![]() 等反应原理,发明了“侯氏制碱法”。
等反应原理,发明了“侯氏制碱法”。
根据侯德榜制碱法原理,实验室用食盐、氨水、犬理石、盐酸制取碳酸钠。其实验过程如下:
 ①配制含氨的氯化钠饱和溶液;②用石灰石和稀盐酸制取纯净的CO2;③将CO2通入NaCl的氨溶液中,得到碳酸氢钠晶体:④过滤,冷水洗涤沉淀;⑤焙烧NaHCO3得到Na2CO3。
①配制含氨的氯化钠饱和溶液;②用石灰石和稀盐酸制取纯净的CO2;③将CO2通入NaCl的氨溶液中,得到碳酸氢钠晶体:④过滤,冷水洗涤沉淀;⑤焙烧NaHCO3得到Na2CO3。
试回答下列问题:
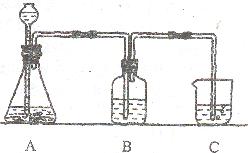
(1)某学生将实验步骤④、③、③设计成下图所示的装置:洗气瓶B中的液体是 ,烧杯C中的液体是 。
(2)实验步骤④中洗涤沉淀的目的是 。
(3)该学生设计右图所示装置进行NaHCO3的分解,并证实产物中有C02产生。
① 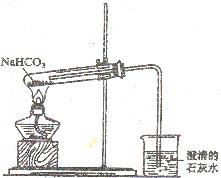 试管中发生的化学反应方程式是:
试管中发生的化学反应方程式是:
②指出该学生设计的装置图的错误之处.并改正(文字说明即可)。
③停止加热时应该怎样操作,为什么?
④烧杯中发生反应的离予方程式是:
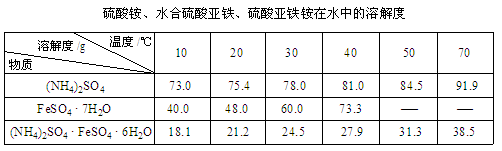
(15分)硫酸亚铁铵又称莫尔盐,是浅绿色晶体。它在空气中比一般亚铁盐稳定,是常用的Fe2+试剂。某实验小组利用工业废铁屑制取莫尔盐,并测定其纯度。
已知:①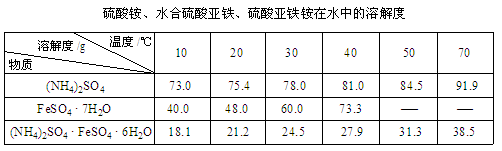
②莫尔盐在乙醇溶剂中难溶。
Ⅰ.莫尔盐的制取
试分析:
(1)步骤2中加热方式 (填“直接加热”﹑“水浴加热”或“沙浴”);必须在铁屑少量剩余时,进行热过滤,其原因是 。
(2)步骤3中包含的实验操作名称 。
(3)产品莫尔盐最后用 洗涤(填字母编号)。
a.蒸馏水 b.乙醇 c.滤液
Ⅱ.为测定硫酸亚铁铵(NH4)2SO4?FeSO4?6H2O晶体纯度,某学生取m g硫酸亚铁铵样品配制成500 mL溶液,根据物质组成,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
(甲)方案一:取20.00 mL硫酸亚铁铵溶液用0.1000 mol·L-1的酸性KMnO4溶液分三次进行滴定。
(乙)方案二:取20.00 mL硫酸亚铁铵溶液进行如下实验。
(1)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为
,验证推测的方法为: 。
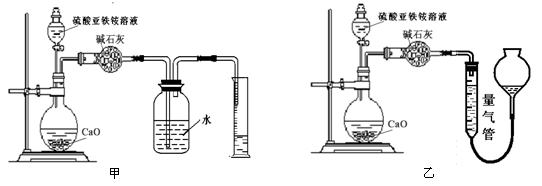
(丙)方案三:(通过NH4+测定)实验设计图如下所示。取20.00 mL硫酸亚铁铵溶液进行该实验。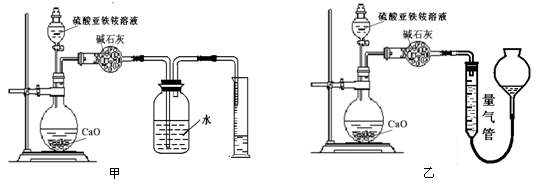
(2)①装置 (填“甲”或“乙”)较为合理,判断理由是 。量气管中最佳试剂是 (填字母编号。如选“乙”则填此空,如选“甲”此空可不填)。
a.水 b.饱和NaHCO3溶液 c.CCl4
②若测得NH3的体积为V L(已折算为标准状况下),则该硫酸亚铁铵晶体的纯度为 。


根据侯德榜制碱法原理,实验室用食盐、氨水、大理石、盐酸制取碳酸钠。其实验过程如下:①配制含氨的氯化钠饱和溶液;②用石灰石和稀盐酸制取纯净的CO2;③将CO2通入NaCl的氨溶液中,得到碳酸氢钠晶体;④过滤,冷水洗涤沉淀;⑤焙烧NaHCO3得到Na2CO3。
试回答下列问题:
(1)某学生将实验步骤①②③设计成下图所示的装置:
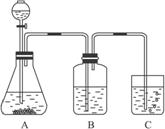
洗气瓶B中的液体是_________,烧杯C中的液体是_________。装置A中的离子方程式是____________________________________。
(2)实验步骤④中过滤操作要求做到“一贴、二低、三靠”,其具体含义是:
一贴:_____________________________________________;
二低:_____________________________________________;
三靠:_____________________________________________。
洗涤沉淀的目的是___________________________________________________________。
(3)该学生设计下图所示装置进行NaHCO3的分解,并证实产物中有CO2产生。
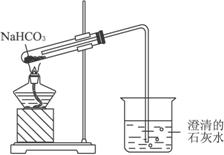
①试管中发生的化学反应方程式是:____________________________________。
②指出该学生设计的装置图的错误之处,并改正(文字说明即可)。
③停止加热时应该怎样操作,为什么?
④烧杯中发生反应的离子方程式是:____________________________________。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com