防止和治理环境污染是当前环保工作的重要研究内容之一。
(1)氮肥厂的氨氮废水经过初步处理后可得到低浓度氨氮废水,后续处理流程如下:
过程I:在硝化细菌作用下,O2将NH4+氧化为NO3-;
过程II:加入甲醇,NO3-和甲醇反应转化CO2和N2。
请写出过程I步的离子方程式:_________________ 。
(2)Hg是水体污染的重金属元素之一。水溶液中二价汞的主要存在形态与Cl-、OH-的浓度关系如图所示[图中的物质或粒子只有Hg(OH)2为难溶物; pCl=-1gc(Cl-)]
①下列说法中正确的是_____________。
A.为了防止Hg
2+水解,配制Hg(NO
3)
2溶液时应将Hg(NO
3)
2固体溶于浓硝酸后再稀释。 B.当c(Cl
-) =10
-1 mol·L
-1时,汞元素一定全部以HgCl
42-形式存在
C.HgCl
2是一种弱电解质,其电离方程式是:HgCl
2=HgCl
+ + Cl
- D.当溶液pH保持在4,pCl由2改变至6时,可使HgCl
2转化为Hg(OH)
2
②HgCl
2又称“升汞”,熔点549K,加热能升华,其晶体是_________(填晶体类型)。
(3)汽车尾气是城市空气污染的一个重要因素,常用以下反应净化汽车尾气:
2NO(g)+2CO(g)

2CO
2(g)+N
2(g) 在某温度T1℃下,2L密闭容器中充入NO 、CO各0.4mol,测得不同时间的NO和CO物质的量如下表:
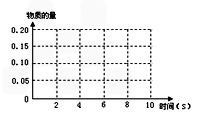
①根据上表的数据,在下图中画出CO2的物质的量与时间的关系曲线。
②上述反应达到平衡后,继续加入NO 、CO、CO2 各0.2mol和N2 __________ mol时,平衡不移动。
③在上述条件下该反应能够自发进行,如果把温度从T1℃升高到T2℃,平衡常数K将__________(填写“变大”、“变小”、“不变”)。
④一种CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似燃料电池,其中的固体电解质是Y2O3-Na2O,O2ˉ可以在其中自由移动,负极的反应式为____________。



 2CO2(g)+N2(g) 在某温度T1℃下,2L密闭容器中充入NO 、CO各0.4mol,测得不同时间的NO和CO物质的量如下表:
2CO2(g)+N2(g) 在某温度T1℃下,2L密闭容器中充入NO 、CO各0.4mol,测得不同时间的NO和CO物质的量如下表: 
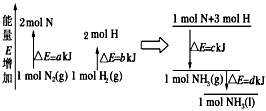
 4FeO+CO2,为制得该种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为____________g。
4FeO+CO2,为制得该种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为____________g。