
题目列表(包括答案和解析)
| 催化剂(0.1g) | 活性炭 | FeCl3 | KI | MnO2颗粒状 | MnO2粉末状 |
| 前15s产生氧气的量(ml) | 5 | 11 | 7 | 8 | 11 |
| 前30s产生氧气的量(ml) | 8 | 16 | 11 | 11 | 21 |
| 前45s产生氧气的量(ml) | 11 | 20 | 15 | 18 | 35 |
| 前60s产生氧气的量(ml) | 15 | 24 | 20 | 26 | 49 |
 有演示实验:用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
有演示实验:用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: |
(10分)某化学兴趣小组在探究次氯酸钠溶液的性质时发现:
往过量FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。
请你协助他们完成该反应还原产物的探究。
(1)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为 。
(2)假设乙同学的推测是正确。
写出过量FeSO4溶液中,滴入几滴NaClO溶液,并加入适量硫酸的离子方程式:
。
请你设计一个实验方案,验证乙同学的推测是正确的。
要求在答题卡上按下表格式写出实验步骤、预期现象和结论(可以不填满):
|
实验操作 |
预期现象和结论 |
|
步骤1:取上述反应后的溶液少许于试管A中,
。 |
|
|
步骤2: 。 |
|
|
步骤3: 。 |
|
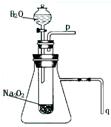
(10分)下面是某研究小组研究的关于不同催化剂对H2O2分解反应的催化效率。
| 催化剂(0.1g) | 活性炭 | FeCl3 | KI | MnO2颗粒状 | MnO2粉末状 |
| 前15s产生氧气的量(ml) | 5 | 11 | 7 | 8 | 11 |
| 前30s产生氧气的量(ml) | 8 | 16 | 11 | 11 | 21 |
| 前45s产生氧气的量(ml) | 11 | 20 | 15 | 18 | 35 |
| 前60s产生氧气的量(ml) | 15 | 24 | 20 | 26 | 49 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com