
题目列表(包括答案和解析)
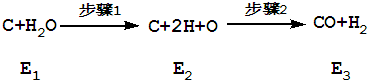

| A.步骤1为吸热反应,步骤2为放热反应 |
| B.E3>E2>E1 |
| C.1mol C发生该反应时吸收的能量为E3-E1 |
| D.E2-E1<E2-E3 |
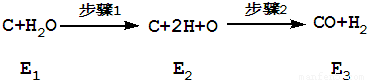
水蒸汽通过灼热的焦炭后,流出的气体的主要成分是CO和H2,还有CO2和水蒸汽等。请用上图中提供的仪器,选择必要的试剂,设计一个实验,证明上述混合气中有CO和H2。(加热装置和导管等略去)
回答下列问题:
(1)盛浓硫酸的装置的用途是
盛NaOH溶液的装置的用途是
(2)仪器B中需加入的试剂的名称(或化学式)是
所发生反应的化学方程式是
(3)仪器C中需加入试剂的名称(或化学式)是
所发生反应的化学方程式是
(4)按气流方向连接各仪器,用字母标示借口的连接顺序:
g a b
(5)能证明混合气体中含有CO的实验依据是:
(6)能证明混合气中含有H2的实验依据是:
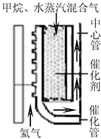 (2010?江苏二模)以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线,主要工艺有以下几种:
(2010?江苏二模)以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线,主要工艺有以下几种:| 1 |
| 2 |
| 气体 | 进口温度/℃ | 进口压强/MPa | 进口流量/g?s-1 | 出口流量/g?s-1 |
| 甲烷 | 464 | 4.26 | 12 | 5.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com