
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
 CH3OH(g);ЎчH=-90.7 kJ/molЈ»
CH3OH(g);ЎчH=-90.7 kJ/molЈ»  CH3OCH3(g) +H2O(g);ЎчH= -23.5 kJ/molЈ»
CH3OCH3(g) +H2O(g);ЎчH= -23.5 kJ/molЈ»  CO2(g)+H2(g);ЎчH=-41.2kJ/molЎЈ
CO2(g)+H2(g);ЎчH=-41.2kJ/molЎЈ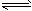 CH3OCH3(g) +CO2(g)Ј¬ФтёГ·ҙУҰөДЎчH=____________
CH3OCH3(g) +CO2(g)Ј¬ФтёГ·ҙУҰөДЎчH=____________ 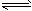 CH3OCH3(g) +3H2O(g)Ј»
CH3OCH3(g) +3H2O(g)Ј»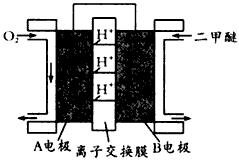
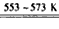 SiHCl3(l)+ H2(g)Ј»
SiHCl3(l)+ H2(g)Ј» Si(ҙҝ) +3HClЎЈ
Si(ҙҝ) +3HClЎЈ
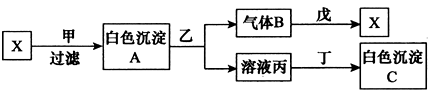
(1)ПВГжБРіцБЛјёЧйОпЦКЈ¬ЗлҪ«ОпЦКөДәПККЧйәЕМоРҙФЪҝХёсЙПЎЈ
Н¬О»ЛШ Ј¬Н¬ПөОп Ј¬Н¬·ЦТм№№Ме ЎЈЈЁМоРҙРтәЕЈ©
ўЩҪрёХКҜУлЎ°ЧгЗтП©ЎұC60Ј» ўЪDУлTЈ» ўЫ16OЎў17OәН18OЈ»
ўЬСхЖшЈЁO2Ј©УліфСхЈЁO3Ј©Ј» ўЭCH4әНCH3CH2CH3Ј»
ўЮТТҙјЈЁCH3CH2OHЈ©әНјЧГСЈЁCH3OCH3Ј©Ј»
ўЯХэ¶ЎНйәНТмОмНй ўа C2H4әНC3H6
(2)ПЦУРјёЦЦУР»ъОпЈәўЩТТП© Ј¬ўЪТТҙјЈ¬ўЫТТЛбЈ¬ўЬТТЛбТТхҘЈ¬ўЭУНЦ¬Ј¬ўЮЖПМСМЗЈ¬
ўЯ өн·Ы Ј¬ ўаө°°ЧЦКЎЈФЪЙПКцУР»ъОпЦРЈЁМоРҙРтәЕЈ©Јә
ўЩДЬ·ўЙъТшҫө·ҙУҰөДКЗ ЎЈўЪДЬ·ўЙъҙЯ»ҜСх»Ҝ·ҙУҰөДКЗ ЎЈ
ўЫДЬ·ўЙъЛ®Ҫв·ҙУҰөДКЗ ЎЈўЬГ»УРЛбРФЗТДЬ·ўЙъхҘ»Ҝ·ҙУҰөДКЗ ЎЈ
ўЭјИДЬ·ўЙъјУіЙ·ҙУҰЈ¬УЦДЬ·ўЙъҫЫәП·ҙУҰөДКЗ ЎЈ
(3)РҙіцПВБРОпЦКөДЧӘ»Ҝ»т·ЦАл·Ҫ·Ё(ГҝТ»ПоЦ»МоРҙТ»ЦЦ·Ҫ·Ё)ЎЈ
(1) °СГәЧӘ»ҜОӘҪ№ВҜЖшЎўГәҪ№УНәНҪ№МҝөИ
(2) Ҫ«ЦШУНЧӘ»ҜОӘЖыУНЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(3) Ҫ«әЈЛ®өӯ»Ҝ
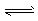 CH3OH(g) ЎчH=-90.7 kJ/mol ўЩ
CH3OH(g) ЎчH=-90.7 kJ/mol ўЩ 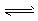 CH3OCH3(g)+H2O(g) ЎчH=-23.5 kJ/molўЪ
CH3OCH3(g)+H2O(g) ЎчH=-23.5 kJ/molўЪ 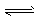 CO2(g)+H2 (g) ЎчH=-41.2 kJ/molўЫ
CO2(g)+H2 (g) ЎчH=-41.2 kJ/molўЫ ¶юјЧГСЈЁCH3OCH3Ј©КЗТ»ЦЦЦШТӘөДҫ«Пё»Ҝ№ӨІъЖ·Ј¬ұ»ИПОӘКЗ¶юК®Т»КАјНЧоУРЗұБҰөДИјБП[ ТСЦӘЈәCH3OCH3(g)+3O2(g)ЈҪ2CO2(g)+3H2OЈЁ1Ј©? ЎчHЈҪЈӯ1455kJ/mol ]ЎЈН¬КұЛьТІҝЙТФЧчОӘЦЖАдјБ¶шМжҙъ·ъВИҙъМюЎЈ№ӨТөЙПЦЖұё¶юјЧГСөДЦчТӘ·Ҫ·ЁҫӯАъБЛИэёцҪЧ¶ОЈә
ўЩјЧҙјТәМеФЪЕЁБтЛбЧчУГПВ»тјЧҙјЖшМеФЪҙЯ»ҜЧчУГПВЦұҪУНСЛ®ЦЖ¶юјЧГСЈ» 2CH3OH  CH3OCH3Ј«H2O
CH3OCH3Ј«H2O
ўЪәПіЙЖшCOУлH2ЦұҪУәПіЙ¶юјЧГСЈә 3H2(g)Ј«3CO(g) CH3OCH3(g)Ј«CO2(g)?? ЎчHЈҪЈӯ247kJ/mol
CH3OCH3(g)Ј«CO2(g)?? ЎчHЈҪЈӯ247kJ/mol
ўЫМмИ»ЖшУлЛ®ХфЖш·ҙУҰЦЖұё¶юјЧГСЎЈТФCH4әНH2OОӘФӯБПЦЖұё¶юјЧГСәНјЧҙј№ӨТөБчіМИзПВЈә
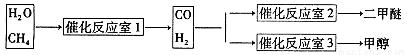
ЈЁ1Ј©РҙіцCO(g)ЎўH2(g)ЎўO2(g)·ҙУҰЙъіЙCO2(g)әНH2OЈЁ1Ј©өДИИ»ҜС§·ҪіМКҪЈЁҪб№ыұЈБфТ»О»РЎКэЈ©????????????????????????????????????????????????
ЈЁ2Ј©ФЪ·ҙУҰКТ2ЦРЈ¬Т»¶ЁМхјюПВ·ўЙъ·ҙУҰ3H2(g)Ј«3CO(g) CH3OCH3(g)Ј«CO2(g)ФЪГЬұХИЭЖчЦРҙпөҪЖҪәвәуЈ¬ТӘМбёЯCOөДЧӘ»ҜВКЈ¬ҝЙТФІЙИЎөДҙлК©КЗ?????
CH3OCH3(g)Ј«CO2(g)ФЪГЬұХИЭЖчЦРҙпөҪЖҪәвәуЈ¬ТӘМбёЯCOөДЧӘ»ҜВКЈ¬ҝЙТФІЙИЎөДҙлК©КЗ?????
AЈ®өНОВёЯС№?? BЈ®јУҙЯ»ҜјБ??? CЈ®ФцјУCOЕЁ¶И?? DЈ®·ЦАліц¶юјЧГС
ЈЁ3Ј©ФЪ·ҙУҰКТ3ЦРЈ¬ФЪТ»¶ЁОВ¶ИәНС№ЗҝМхјюПВ·ўЙъБЛ·ҙУҰЈә3H2(g)Ј«CO2(g)  CH3OH(g)Ј«H2O (g)? ЎчHЈј0·ҙУҰҙпөҪЖҪәвКұЈ¬ёДұдОВ¶ИЈЁTЈ©әНС№ЗҝЈЁPЈ©Ј¬·ҙУҰ»мәПОпCH3OHЎ°ОпЦКөДБҝ·ЦКэЎұұд»ҜЗйҝцИзНјЛщКҫЈ¬№ШУЪОВ¶ИЈЁTЈ©әНС№ЗҝЈЁPЈ©өД№ШПөЕР¶ПХэИ·өДКЗ??? ЈЁМоРтәЕЈ©
CH3OH(g)Ј«H2O (g)? ЎчHЈј0·ҙУҰҙпөҪЖҪәвКұЈ¬ёДұдОВ¶ИЈЁTЈ©әНС№ЗҝЈЁPЈ©Ј¬·ҙУҰ»мәПОпCH3OHЎ°ОпЦКөДБҝ·ЦКэЎұұд»ҜЗйҝцИзНјЛщКҫЈ¬№ШУЪОВ¶ИЈЁTЈ©әНС№ЗҝЈЁPЈ©өД№ШПөЕР¶ПХэИ·өДКЗ??? ЈЁМоРтәЕЈ©
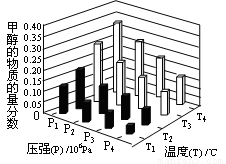
AЈ®P3ЈҫP2?? T3ЈҫT2?????? BЈ®P2ЈҫP4?? T4ЈҫT2
CЈ®P1ЈҫP3 ? T1ЈҫT3?????? DЈ®P1ЈҫP4?? T2ЈҫT3
ЈЁ4Ј©·ҙУҰКТ1ЦР·ўЙъ·ҙУҰЈәCH4(g)Ј«H2O(g) CO(g)Ј«3H2(g)? ЎчHЈҫ0РҙіцЖҪәвіЈКэөДұнҙпКҪЈә??????????????????????????
CO(g)Ј«3H2(g)? ЎчHЈҫ0РҙіцЖҪәвіЈКэөДұнҙпКҪЈә??????????????????????????
Из№ыОВ¶ИҪөөНЈ¬ёГ·ҙУҰөДЖҪәвіЈКэ????????????? ЈЁМоЎ°І»ұдЎұЎўЎ°ұдҙуЎұЎўЎ°ұдРЎЎұЈ©
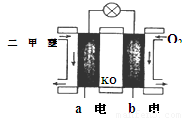
ЈЁ5Ј©ИзНјОӘВМЙ«өзФҙЎ°¶юјЧГСИјБПөзіШЎұөД№ӨЧчФӯАнКҫТвНјФтaөзј«өД·ҙУҰКҪОӘЈә________________
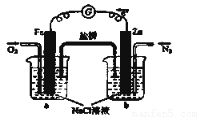
ЈЁ6Ј©ПВБРЕР¶ПЦРХэИ·өДКЗ_______
AЈ®ПтЙХұӯaЦРјУИлЙЩБҝK3[Fe(CN)6]ИЬТәЈ¬УРА¶Й«іБөнЙъіЙ
BЈ®ЙХұӯbЦР·ўЙъ·ҙУҰОӘ2Zn-4eЎҘ ЈҪ2Zn2+
CЈ®өзЧУҙУZnј«БчіцЈ¬БчИлFeј«Ј¬ҫӯСОЗЕ»ШөҪZnј«
DЈ®ЙХұӯaЦР·ўЙъ·ҙУҰO2 + 4H+ + 4eЎҘ ЈҪ 2H2OЈ¬ИЬТәpHҪөөН
ЈЁ14·ЦЈ©¶юјЧГСЈЁCH3OCH3Ј©әНјЧҙјЈЁCH3OHЈ©¶јКЗёЯР§ЗеҪаДЬФҙЎЈ№ӨТөЙПАыУГГәөДЖш»ҜІъОпЈЁЛ®ГәЖшЈ©әПіЙјЧҙјәН¶юјЧГСЎЈ»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ЦЖұё¶юјЧГСЧоәуТ»ІҪ·ҙУҰУЙAl2O3ҙЯ»ҜјЧҙјНСЛ®әПіЙЈ¬·ҙУҰ·ҪіМКҪОӘ ЎЈ
ЈЁ2Ј©ТСЦӘЈәCO(g)+2H2(g)=CH3OH (g) ЎчH= ЎӘ90.1kJЎӨmol-1 CO(g)өДИјЙХИИКЗ282.8 kJЎӨmol-1Ј»H2өДИјЙХИИКЗ285.8 kJЎӨmol-1РҙіцұнКҫCH3OH (g) ИјЙХИИөДИИ»ҜС§·ҙУҰ·ҪіМКҪ ЎЈ
ЈЁ3Ј©¶юјЧГСЦұҪУИјБПөзіШұИјЧҙјЦұҪУИјБПөзіШёьёЯР§Ј¬өИЦКБҝөД¶юјЧГСәНјЧҙјНкИ«·ЕөзЧӘТЖөзЧУөДОпЦКөДБҝЦ®ұИКЗ ЎЈУГ¶юјЧГСЦұҪУИјБПөзіШөзҪвЧгБҝұҘәНКіСОЛ®Ј¬өұПыәД9.2g¶юјЧГСКұАнВЫЙПТхј«ІъЙъөДЖшМеөДМе»эОӘ LЎЈЈЁұкҝцПВЈ©
ЈЁ4Ј©ФЪәПіЙЦР°йУРЛ®ГәЖшҪ»»»·ҙУҰЈәCO(g)+H2O(g)  CO2(g)+H2(g)Ј¬өИОпЦКөДБҝөДCO(g)әНH2O(g)јУИлГЬұХИЭЖчЦР·ҙУҰЈ¬ЖҪәвКұІвөГҪб№ыИзПВұнЎЈ
CO2(g)+H2(g)Ј¬өИОпЦКөДБҝөДCO(g)әНH2O(g)јУИлГЬұХИЭЖчЦР·ҙУҰЈ¬ЖҪәвКұІвөГҪб№ыИзПВұнЎЈ
| ОВ¶И | 260Ўж | 280Ўж | 295Ўж | 310Ўж |
| COЧӘ»ҜВК | 89% | 80% | 75% | 60% |
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com