
题目列表(包括答案和解析)
2![]() +5
+5![]() +H+====2Mn2++5
+H+====2Mn2++5![]() +3H2O
+3H2O
填空回答问题:
(1)该滴定实验所需仪器有下列中的______________(填序号)。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL)
C.量筒(10 mL) D.锥形瓶
E.铁架台 F.滴定管夹
G.烧杯 H.白纸
I.胶头滴管 J.漏斗
(2)不用___________(填写“酸”“碱”)式滴定管盛装高锰酸钾溶液,试分析原因:
____________________________。
(3)选何种指示剂,说明理由________________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL。则(b-a) mL,比实际消耗KMnO4溶液体积_________(多、少),根据(b-a) mL计算,得到的待测浓度,比实际浓度________(大、小)。
氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应离子方程式是2 +
+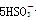 +H+===2Mn2++5
+H+===2Mn2++5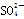 +3H2O,填空回答问题:
+3H2O,填空回答问题:
(1)该滴定实验所需仪器有下列中的________(填序号)。
| A.酸式滴定管(50 mL) | B.碱式滴定管(50 mL) |
| C.量筒(10 mL) | D.锥形瓶 |
氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001 mol·L-1酸性KMnO4溶液和未知浓度的无色NaHSO3溶液。反应的离子方程式是2MnO4-+5HSO3-+H+]2Mn2++5SO42-+3H2O。填空回答问题:
(1)该滴定实验所需仪器为下列中的__________。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL)
C.量筒(10 mL) D.锥形瓶 E.铁架台 F.滴定管夹
G.烧杯 H.白纸 I.胶头滴管 J.漏斗
(2)不用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因:________________________________________________________________________
________________________________________________________________________。
(3)选何种指示剂,说明理由
________________________________________________________________________
________________________________________________________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积________(填“多”或“少”)。根据(b-a)mL计算得到的待测浓度,比实际浓度________(填“大”或“小”)。
氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001 mol·L-1酸性KMnO4溶液和未知浓度的无色NaHSO3溶液,反应离子方程式是2MnO4-+5HSO3-+H+===2Mn2++5SO42-+3H2O。填空回答问题:
(1)该滴定实验所需仪器有下列中的________。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL)
C.量筒(10 mL) D.锥形瓶
E.铁架台 F.滴定管夹
G.烧杯 H.白纸
I.胶头滴管 J.漏斗
(2)不能用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因:________________________________________________________________________
__________________________。
(3)选何种指示剂,说明理由
________________________________________________________________________
__________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a) mL比实际消耗KMnO4溶液体积________(填“多”或“少”)。根据(b-a) mL计算得到的待测浓度,比实际浓度________(填“大”或“小”)。
氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001 mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应离子方程式是2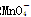 +
+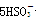 +H+===2Mn2++5
+H+===2Mn2++5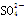 +3H2O,填空回答问题:
+3H2O,填空回答问题:
(1)该滴定实验所需仪器有下列中的________(填序号)。
A.酸式滴定管(50 mL) B.碱式滴定管(50 mL)
C.量筒(10 mL) D.锥形瓶
E.铁架台 F.滴定管夹
G.烧杯 H.白纸
I.胶头滴管 J.漏斗
(2)不用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因:
________________________________________________________________________。
(3)选何种指示剂,说明理由
________________________________________________________________________。
(4)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积偏________(填“多”或“少”)。根据(b-a) mL计算得到的待测浓度,比实际浓度偏________(填“大”或“小”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com