
题目列表(包括答案和解析)
工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) ΔH<0
Si3N4(s)+12HCl(g) ΔH<0
某温度和压强条件下,分别将0.3 mol SiCl4(g)、0.2 mol N2(g)、0.6 mol H2(g)充入2 L密闭容器内,进行上述反应,5 min达到平衡状态,所得Si3N4(s)的质量是5.60 g。
(1)H2的平均反应速率是 mol·L-1·min-1。
(2)平衡时容器内N2的浓度是 mol·L-1。
(3)SiCl4(g)的转化率是 。
(4)若按n(SiCl4)∶n(N2)∶n(H2)=3∶2∶6的投料配比,向上述容器不断扩大加料,SiCl4(g)的转化率应 (填“增大”“减小”或“不变”)。
(5)在不改变反应条件的情况下,为了提高SiCl4(g)的转化率,可通过改变投料配比的方式来实现。下列四种投料方式,其中可行的是 。
选项投料方式
An(SiCl4)∶n(N2)∶n(H2)=1∶1∶2
Bn(SiCl4)∶n(N2)∶n(H2)= 1∶2∶2
Cn(SiCl4)∶n(N2)∶n(H2)= 3∶2∶2
Dn(SiCl4)∶n(N2)∶n(H2)= 2∶1∶3
(6)达到平衡后升高温度,其他条件不变,对平衡体系产生的影响是 (填字母序号)。
A.c(HCl)减少
B.正反应速率减慢,逆反应速率加快
C.Si3N4的物质的量减小
D.重新平衡时c(H2)/c(HCl)增大
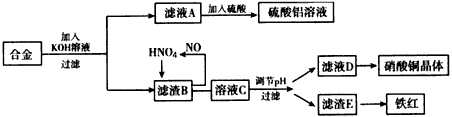

请完成下列问题:
(1)已知M的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则M的分子式是_________。D是双原子分子,相对分子质量为30,则D的分子式为_________。
(2)油脂A经下列途径可得到M。
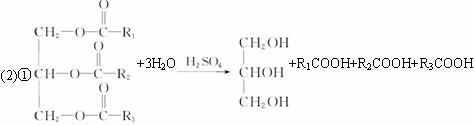
上框图中②的提示:
C2H5OH+HNO![]() C2H5ONO2+H2O
C2H5ONO2+H2O
硝酸乙酯
反应①的化学方程式是__________。
反应②的化学方程式是__________。
(3)C是B和乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式_________。
(4)若将0.1 mol B与足量的金属钠反应,则需消耗__________g金属钠。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com