
题目列表(包括答案和解析)
合成氮反应的正反应是气体体积减小的放热反应。合成氨工业的生成流程如下:
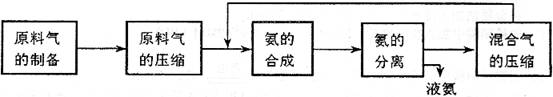
关于合成氨工业的说法中不正确的是
A.混合气进行循环利用遵循绿色化学思想
B.合成氨反应须在低温下进行
C.对原料气进行压缩是为了增大原料气的转化率
D.使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动
氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位。工业制硝酸的主要反应之一是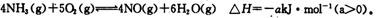
(1)如果将4mol NH3和5mol O2放入容器中,达到平衡时放出热量0.8akJ,则平衡时NH3的转化率为 。
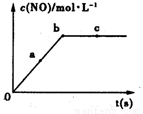
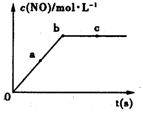
(2)在一定条件下,容积固定的密闭容器中进行上述反应,NO的浓度与时间关系如图所示,则NO的a、b、c三点的反应速率v(a正)、v(b逆)、v(c正)的大小关系是 。
(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表:
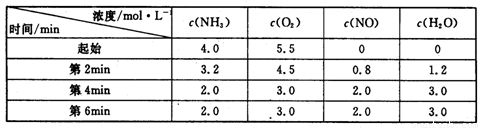
①第2min到第4mim,反应速率v(O2)= ;
②第2min时改变了条件,改变的条件可能是 (从所给选项中选择);
A.降低温度 B.增加了生成物 C.减小压强 D.使用了高效催化剂
③在与第4min相同的温度下,若起始向容器中加入NH3、O2、NO和H2O(g)的浓度都为2moI/L,则该反应 (填“正反应方向进行”、“逆反应方向进行”、“不移动”)。
(4)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气。尿素(H2NCONH2)是一种非常重要的高氮化肥,在温度70—95℃时,工业尾气中的NO、NO2可以用尿素溶液吸收,将其转化为N2,尿素与NO、NO2三者等物质的量反应的化学方程式为 。
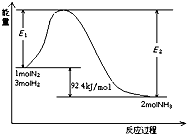
(5)目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
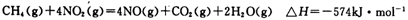
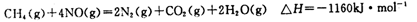
则1mol甲烷直接将NO2还原为N2的烩变为____ 。
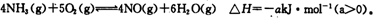

| A.降低温度 | B.增加了生成物 | C.减小压强 | D.使用了高效催化剂 |
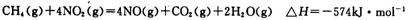
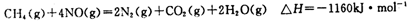
 在一定体积的密闭容器中,进行如下化学反应:
在一定体积的密闭容器中,进行如下化学反应:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| [CO]?[H2O] |
| [CO2]?[H2] |
| [CO]?[H2O] |
| [CO2]?[H2] |
A.一定没有氮气,但一氧化碳和氯化氢至少有一种
B.一定有氮气,且一氧化碳和氯化氢至少有一种
C.一定有氮气和氯化氢,但没有一氧化碳
D.混合气体中一定含有氮气、一氧化碳和氯化氢
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com