
题目列表(包括答案和解析)
 图中表示外界条件(t、p)的变化对下列可逆反应的影响:
图中表示外界条件(t、p)的变化对下列可逆反应的影响:
L(s)+G(g)![]() 2R(g);△H>0,y 轴表示的是 ( )
2R(g);△H>0,y 轴表示的是 ( )
A. 平衡时,混合气中G的百分含量 B. G的转化率
C. 平衡时,混合气中R的百分含量 D. L的转化率
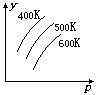 图中表示外界条件(t、p)的变化对下列可逆反应的影响:
图中表示外界条件(t、p)的变化对下列可逆反应的影响: 2R(g);△H>0,y 轴表示的是 ( )
2R(g);△H>0,y 轴表示的是 ( )| A.平衡时,混合气中G的百分含量 | B.G的转化率 |
| C.平衡时,混合气中R的百分含量 | D.L的转化率 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com