Ⅰ.下列实验操作中,合理的是
AC
AC
A.实验室制乙烯时,在酒精和浓硫酸的混合液中,放入几片碎瓷片,加热混合物,使液体温度迅速升到170℃
B.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置,待液体分层后,滴加硝酸银溶液
C.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入无水乙醇中,完成乙醇氧化为乙醛的实验
D.苯酚中滴加少量稀溴水,可用来定量检验苯酚
E.工业酒精制取无水酒精时,先加生石灰然后蒸馏,蒸馏必须将温度计的水银球插入反应液中,测定反应液温度
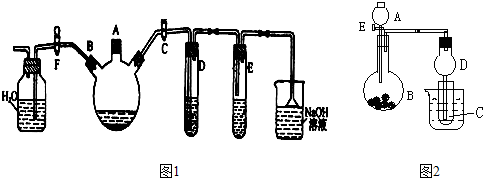
Ⅱ.实验室用图1所示装置制备溴苯,并验证该反应是取代反应.
(1)关闭F活塞,打开C活塞,在装有少量苯的三颈瓶中由A口加入少量溴,再加入少量铁屑,塞住A口,则三颈瓶中发生反应的化学方程式为:
.
(2)D试管内装的是
CCl4
CCl4
,其作用是
吸收挥发出的苯蒸汽和溴
吸收挥发出的苯蒸汽和溴
.
(3)E试管内装的是
AgNO3溶液
AgNO3溶液
,E试管内出现的现象为
导管口产生大量白雾,生成淡黄色沉淀
导管口产生大量白雾,生成淡黄色沉淀
.
(4)待三口烧瓶中的反应即将结束时(此时气体明显减少),打开F活塞,关闭C活塞,可以看到的现象是
水倒吸至三口烧瓶中
水倒吸至三口烧瓶中
.
(5)上一步得到粗溴苯后,要用如下操作精制:
a蒸馏; b水洗; c用干燥剂干燥; d 10%NaOH溶液洗涤; e水洗
正确的操作顺序是
bdeca(或edbca)
bdeca(或edbca)
Ⅲ.用如图2所示装置进行实验,将A逐滴加入B中:
(1)若B为Na
2CO
3粉末,C为C
6H
5ONa溶液,实验中观察到小试管内溶液由澄清变浑浊,则试管C中化学反应的离子方程式:
.然后往烧杯中加入沸水,可观察到试管C中的现象:
溶液由浑浊变澄清
溶液由浑浊变澄清
.
(2)若B是生石灰,观察到C溶液中先形成沉淀,然后沉淀溶解.当沉淀完全溶解,恰好变澄清时,关闭E.然后往小试管中加入少量乙醛溶液,再往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是
浓氨水
浓氨水
(填名称),C是
AgNO3
AgNO3
(填化学式),与乙醛的混合后,该溶液中反应的化学方程式:
CH
3CHO+2Ag(NH
3)
2OH

CH
3COONH
4+H
2O+2Ag↓+3NH
3CH
3CHO+2Ag(NH
3)
2OH

CH
3COONH
4+H
2O+2Ag↓+3NH
3.仪器D在此实验中的作用是
防止倒吸
防止倒吸
.

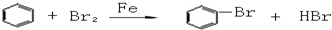
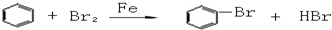
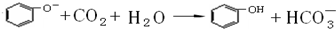
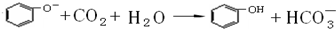
 CH3COONH4+H2O+2Ag↓+3NH3
CH3COONH4+H2O+2Ag↓+3NH3 CH3COONH4+H2O+2Ag↓+3NH3
CH3COONH4+H2O+2Ag↓+3NH3