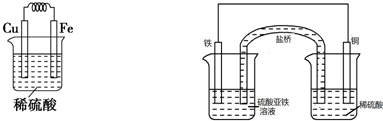
某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
方案Ⅰ:有人提出将形状和大小均相等的铁片和铜片,分别同时放入100ml2.0mol/L稀硫酸中,观察产生气泡的快慢,据此可以确定它们的金属活动性.该原理的离子方程式为:
Fe+2H+═Fe2++H2↑;
Fe+2H+═Fe2++H2↑;
;若反应进行到2min时共收集到标准状况下的气体1120ml,则用硫酸表示的该反应的反应速率为(溶液体积变化忽略不计):
0.25mol/(L?min)
0.25mol/(L?min)
.
方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性.试在下面的方框内画出你设计的原电池装置图,注明电解质溶液名称和正负极材料,标出电子流动方向,并写出电极反应式.
正极反应式:
2H++2e-═H2↑
2H++2e-═H2↑
.
负极反应式:
Fe-2e-═Fe2+
Fe-2e-═Fe2+
.
方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案(与方案Ⅰ、Ⅱ不能雷同):
将铁片置于CuSO4溶液中,一段时间后观察Fe表面有红色的金属铜析出,即可以证明金属铁的活泼性强于金属铜的
将铁片置于CuSO4溶液中,一段时间后观察Fe表面有红色的金属铜析出,即可以证明金属铁的活泼性强于金属铜的
,用离子方程式表示其反应原理:
Fe+Cu2+═Fe2++Cu
Fe+Cu2+═Fe2++Cu
.

 某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目: