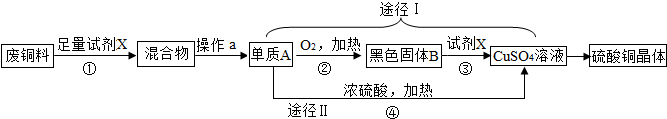
硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂.以下是由废铜料(含铁)生产硫酸铜晶体的流程
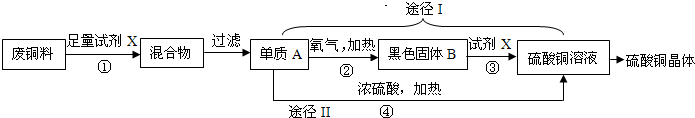
(1)反应①的化学方程式为
.
(2)途径I中,反应②、③的化学方程式分别为②
,③
;途径Ⅱ中,反应④的化学方程式为Cu+2H
2SO
4(浓)
CuSO
4+SO
2↑+2H
2O.从环保和经济的角度分析,利用途径
(选填“I”或“Ⅱ”)制取硫酸铜的方案更合理.
(3)某化学兴趣小组同学用足量铜与10g质量分数为98%的浓硫酸在加热条件下充分反应,生成SO
2的质量应
(选填字母).
A.等于3.2g B.小于3.2g C.大于3.2g
(4)该化学兴趣小组同学通过查阅资料,发现大多数金属与浓硫酸都能发生反应.现取足量锌与浓硫酸反应,其化学方程式为:Zn+2H
2SO
4(浓)═ZnSO
4+SO
2↑+2H
2O.反应一段时间后,老师指出除了SO
2,还可能生成另一种气体.请你根据锌的化学性质,推断此气体可能是
,理由是
.