
题目列表(包括答案和解析)
三种气体的实验室制法以及它们的区别
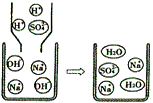 氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题.
氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题.| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |
| 实验步骤及操作 | 实验现象 | 实验结论 |
| 取样于试管中,加入足 量蒸馏水振荡,静置 ①取上层清液,滴入 无色酚酞试液 ②倒去上层清液,再向 试管中注入稀盐酸 |
若:①无色酚酞试液不变红 ②有气泡产生 |
全部变质 |
| 若:①无色酚酞试液变红 ② 有气泡产生 有气泡产生 |
部分变质 部分变质 | |
| 若:① 无色酚酞试液变红 无色酚酞试液变红 ②没有气泡产生 |
没有变质 没有变质 |
| 实验步骤及操作 | 实验现象 | 实验结论 |
| 取样于试管中,加入足 量蒸馏水振荡,静置 ①取上层清液,滴入 无色酚酞试液 ②倒去上层清液,再向 试管中注入稀盐酸 | 若:①无色酚酞试液不变红 ②有气泡产生 | 全部变质 |
| 若:①无色酚酞试液变红 ②______ | ______ | |
| 若:①______ ②没有气泡产生 | ______ |
| 实验步骤及操作 | 实验现象 | 实验结论 |
| 取样于试管中,加入足 量蒸馏水振荡,静置 ①取上层清液,滴入 无色酚酞试液 ②倒去上层清液,再向 试管中注入稀盐酸 |
若:①无色酚酞试液不变红 ②有气泡产生 |
全部变质 |
| 若:①无色酚酞试液变红 ②______ |
______ | |
| 若:①______ ②没有气泡产生 |
______ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com