
题目列表(包括答案和解析)
围绕下列七种物质:①铝,②A12O3,③稀硝酸,④H2SO4,⑤Ba(OH)2固体,⑥氨水,⑦A12(SO4)3,根据要求回答下列问题。
(1)既能与强酸反应,又能与强碱反应的是 (填序号)。
(2)属于电解质的是 (填序号)。
(3)写出最适宜制取Al(OH)3的离子方程式 。
(4)两物质发生反应的离子方程式为H++OH—=H2O,请写出该反应的化学方程式 。
(5)34.2g⑦溶于水配成500mL溶液,溶液中SO42—的物质的量浓度为 。
(6)①与③发生反应的化学方程式为A1+4HNO3=A1(NO3)3+NO↑+2H2O,该反应中还原剂与氧化剂的物质的量之比是 。
围绕下列七种物质:①铝,②A12O3,③稀硝酸,④H2SO4,⑤Ba(OH)2固体,⑥氨水,⑦A12(SO4)3,根据要求回答下列问题。
(1)既能与强酸反应,又能与强碱反应的是 (填序号)。
(2)属于电解质的是 (填序号)。
(3)写出最适宜制取Al(OH)3的离子方程式 。
(4)两物质发生反应的离子方程式为H++OH—=H2O,请写出该反应的化学方程式 。
(5)34.2g⑦溶于水配成500mL溶液,溶液中SO42—的物质的量浓度为 。
(6)①与③发生反应的化学方程式为A1+4HNO3=A1(NO3)3+NO↑+2H2O,该反应中还原剂与氧化剂的物质的量之比是 。
 (2012?百色二模)A、B、C、D均为中学化学中的物质.它们间的反应关系如右图所示.
(2012?百色二模)A、B、C、D均为中学化学中的物质.它们间的反应关系如右图所示.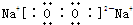
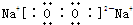
| 7 |
| 2 |
| 7 |
| 2 |
现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复):H+、Na+、A13+、Ag+、Ba2+、OH—、C1—、CO32—、NO3—、SO42—
已知:
①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀。
④在E溶液中逐滴加入B溶液,溶液先出现沉淀,当滴加至过量时,沉淀部分溶解。
试回答下列问题:
(1)A、C的化学式分别为 、 。
(2)A溶液呈碱性的原因 (用离子方程式表示)。
(3)在100mL0.1mol·L-1的E溶液中,逐滴加入35mL 2mol·L-1NaOH溶液,最终得到沉淀的物质的量为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com