
题目列表(包括答案和解析)
甲、乙、丙、丁、戊共五种烃各取1mol,分别在足量的氧气中充分燃烧,得到的二氧化碳的质量相等。
(1)甲、乙能使溴水褪色,其中乙可与氢气反应生成甲,进一步与氢气反应可生成丙;
(2)丙不能与溴水反应,也不能使酸性KMnO4溶液褪色;
(3)丁在铁存在下可与液溴反应,但不能使溴水或酸性KMnO4溶液褪色;
(4)丁可与氢气在一定条件下加成并生成戊,戊不能使酸性KMnO4溶液褪色;
(5)甲燃烧后生成的CO2在标准状况下的体积为134.4L,则:
①甲~戊的分子式依次为甲:________;乙:_____________;丙:________;丁:________;戊:________;
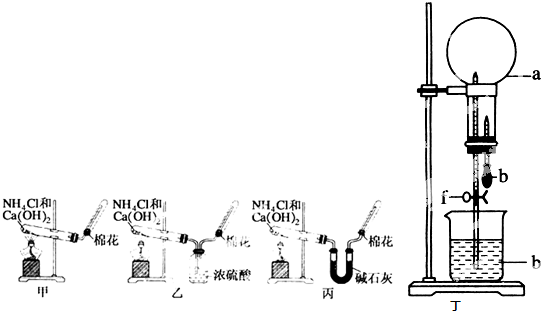
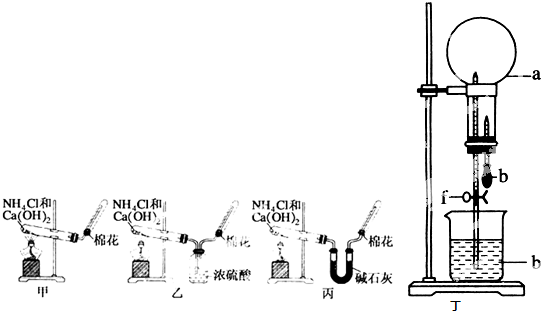
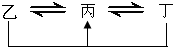 元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:
元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com