
题目列表(包括答案和解析)
在3H2(g)+N2(g)  2NH3(g)的反应中,经过一段时间后,NH3的浓度增加了0.6mol·L-1,此时间内用H2表示的平均速率为0.45mol·L-1·s-1,则这段时间是
2NH3(g)的反应中,经过一段时间后,NH3的浓度增加了0.6mol·L-1,此时间内用H2表示的平均速率为0.45mol·L-1·s-1,则这段时间是
A. 1s B. 0.44s C. 1.33s D. 2s
在3H2(g)+N2(g) 2NH3(g)的反应中,经过一段时间后,NH3的浓度增加了0.6mol·L-1,此时间内用H2表示的平均速率为0.45mol·L-1·s-1,则这段时间是
A. 1s B.0.44s C. 1.33s D. 2s
|
在3H2(g)+N2(g) | |
| [ ] | |
A. |
1 s |
B. |
0.44 s |
C. |
1.33 s |
D. |
2 s |
 合成氨反应是“将空气变成面包”的反应,如果没有合成氨反应,地球将无法养活现在这么多的人.已知合成氨的反应为N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1.
合成氨反应是“将空气变成面包”的反应,如果没有合成氨反应,地球将无法养活现在这么多的人.已知合成氨的反应为N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1. CO(g)+H2(g)△H=+131.3kJ?mol-1,
CO(g)+H2(g)△H=+131.3kJ?mol-1,| 化学键 | C-O | C-H | H-H | C≡O | O-H |
| 键能 kg/mol-1 | 358 | 413 | 436 | 1072 | 463 |
 2NH3(g)△H=-92.4kJ/mol
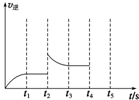
2NH3(g)△H=-92.4kJ/mol 在一体积不变的容器中,当合成氨反应达到平衡后,在t1时升高温度,t2重新达到平衡,t3时充入氮气,t4时重新达到平衡,t5时移去一部分产物,t6时又达到平衡,请在下面的反应速率与时间关系图中画出t1到t5逆反应速率、t5到t6正反应速率的变化情况.
在一体积不变的容器中,当合成氨反应达到平衡后,在t1时升高温度,t2重新达到平衡,t3时充入氮气,t4时重新达到平衡,t5时移去一部分产物,t6时又达到平衡,请在下面的反应速率与时间关系图中画出t1到t5逆反应速率、t5到t6正反应速率的变化情况.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com