(2010?大连二模)燃料电池是一种连续的将燃料和氧化剂的化学能直接转化为电能的化学电池,除氢气外,烃、肼、甲醇等液体或气体,均可以作燃料电池的燃料.请回答下列问题:
(1)以甲烷和氧气为原料,氢氧化钠溶液为电解质溶液构成电池.写出其正极反应式
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.
(2)以上述电池为电源,通过导线与图1电解池相连.
(Ⅰ)X、Y为石墨,a为1L0.1mol/L的氯化钾溶液,写出电解总反应的离子方程式
.
(II)X、Y分别为铁、铜,a为1L0.1mol/L硫酸铜溶液,写出X电极反应式
Cu2++2e-=Cu
Cu2++2e-=Cu
.
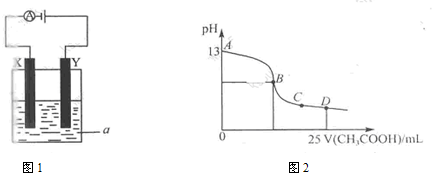
(3)室温时,按(I)电解一段时间后,取25mL上述电解后溶液,滴加0.2mol/L醋酸得到图2(不考虑能量损失和气体溶于水,溶液体积变化忽略不计).
①结合图2计算消耗标准状况下甲烷
280
280
mL.
②若图2的B点pH=7,则酸碱恰好完全反应的点是
AB
AB
区间(填“AB”、“BC”或“CD”).
③AB区间溶液中各离子浓度大小关系是
c(K+)>c(OH-)>c(CH3COO-)>c(H+)或c(K+)>c(CH3COO-)>c(OH-)>c(H+)或 c(K+)>c(CH3COO-)=c(OH-)>c(H+)
c(K+)>c(OH-)>c(CH3COO-)>c(H+)或c(K+)>c(CH3COO-)>c(OH-)>c(H+)或 c(K+)>c(CH3COO-)=c(OH-)>c(H+)
.



 按图装置进行实验,并回答下列问题
按图装置进行实验,并回答下列问题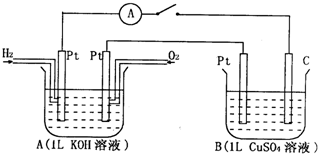
 如图:如图:通电5min后,电极5质量增加2.16g,试回答:
如图:如图:通电5min后,电极5质量增加2.16g,试回答: