
题目列表(包括答案和解析)
(1)实验室制取硫化氢的化学方程式____________________________________。
(2)根据装置图完成下列问题。

①制取硫化氢气体的发生装置可以选用_____________。
②若用C装置收集硫化氢气体,进气口应为_____________,原因是___________________。
③为了验证硫化氢的水溶液呈酸性,可以将气体通入装置D,D中所盛的试剂应该是_____________,现象是_______________________。
④做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置E吸收,E中漏斗的作用为____________________________。
⑤整套装置的连接口连接顺序为(填写a、b、c等符号)____________________。
(3)现用
①收集到的H2S气体的体积(标准状况)。
②溶液中Fe2+和H+的物质的量浓度。
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、
减少酸雨和光化学烟雾的有效途径。
⑴ 有效“减碳”的手段之一是节能。下列制氢方法最节能的是 ▲ 。(填字母序号)
A.电解水制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O![]() CO+3H2
CO+3H2
⑵ CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 molCO2和3 mol H2,一定
条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,测得CO2 和CH3OH(g)
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,测得CO2 和CH3OH(g)
的浓度随时间变化如下图所示。
①从3 min到10 min,v(H2)= ▲ mol·L-1·min-1。(保留2位有效数字)
 ②能说明上述反应达到平衡状态的是 ▲ (选填编号)。
②能说明上述反应达到平衡状态的是 ▲ (选填编号)。
A.反应中CO2与CH3OH的物质的量浓度相等
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
⑶ 新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产
物反应。该技术的优点除了能回收利用SO2外,还能得到一种正盐作为复合肥料。该复合肥料的化
 学式为 ▲ 。
学式为 ▲ 。
⑷ 在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、
NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。某研究性学习小组探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 ▲ 时,催化剂对汽车尾气的催化效果最好。(填a、b、c、d)
(10分)CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。

(1)有效“减碳”的手段之一是节能。下列制氢方法最节能的是 ▲ 。(填字母序号)
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O CO+3H2
CO+3H2
(2)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 molCO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH="-49.0" kJ/mol,测得CO2 和CH3OH(g)的浓度随时间变化如上图所示。
CH3OH(g)+H2O(g) ΔH="-49.0" kJ/mol,测得CO2 和CH3OH(g)的浓度随时间变化如上图所示。
①从3 min到10 min,v(H2)= ▲ mol/(L·min)-1。
②能说明上述反应达到平衡状态的是 ▲ (选填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1︰1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为 ▲ (只要求写一种)。
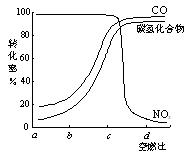
(4)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。某研究性学习小组探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 ▲ 时,催化剂对汽车尾气的催化效果最好。(填a、b、c、d)


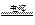 2H2↑+O2↑
2H2↑+O2↑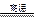 2H2↑+O2↑
2H2↑+O2↑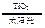 2H2↑+O2↑
2H2↑+O2↑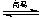 CO+3H2
CO+3H2 CH3OH(g)+H2O(g) ΔH="-49.0" kJ/mol,测得CO2 和CH3OH(g)的浓度随时间变化如上图所示。
CH3OH(g)+H2O(g) ΔH="-49.0" kJ/mol,测得CO2 和CH3OH(g)的浓度随时间变化如上图所示。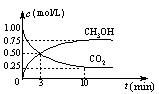
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)有效“减碳”的手段之一是节能。下列制氢方法最节能的是 ▲ 。(填字母序号)
A.电解水制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O![]() CO+3H2
CO+3H2
(2)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 molCO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,测得CO2 和CH3OH(g)的浓度随时间变化如上图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,测得CO2 和CH3OH(g)的浓度随时间变化如上图所示。

①从3 min到10 min,v(H2)= ▲ mol/(L·min)-1。
②能说明上述反应达到平衡状态的是 ▲ (选填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1︰1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为 ▲ (只要求写一种)。
(4)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。某研究性学习小组探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为 ▲ 时,催化剂对汽车尾气的催化效果最好。(填a、b、c、d)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com