
题目列表(包括答案和解析)
| A、W10O21 | B、W10O27 | C、W8O22 | D、W5O14 |
取20g混有二氧化锰的氯酸钾,加热至恒重.在一定温度下,将残留的固体加入10g水中,有7.9g固体未溶解,再加入5g水仍有5.3g固体未溶.则原混合物中可能含有的![]() 质量为
质量为
[ ]
A.14.7g B.6.9g C.12.1g D.17.6g
|
现有7.9 g锰的氧化物跟足量浓盐酸反应,共收集到Cl2 3.55 g,则该反应是 | |
| [ ] | |
A. |
Mn2O3+6HCl=2MnCl2+3H2O+Cl2↑ |
B. |
Mn3O4+8HCl=3MnCl2+4H2O+Cl2↑ |
C. |
MnO2+4HCl=MnCl2+2H2O+Cl2↑ |
D. |
Mn2O7+14HCl=2MnCl2+7H2O+5Cl2↑ |
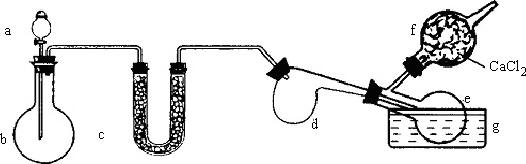
用下图装置(酒精灯、铁架台等未画)制取三氯化磷,在曲颈甑d中放入足量白磷,将![]() 迅速而不间断地通入曲颈甑中,
迅速而不间断地通入曲颈甑中,![]() 与白磷就发生反应,产生火焰.
与白磷就发生反应,产生火焰.
![]() 和
和![]() 熔点分别是-112℃,148℃,沸点分别是76℃,200℃.
熔点分别是-112℃,148℃,沸点分别是76℃,200℃.
(1)现有浓盐酸、浓硫酸、白磷、二氧化锰、氢氧化钠供选用,a、b中应装入的试剂分别为:a_________,b__________.
(2)需加热的仪器是________(填仪器字母).
(3)生成的![]() 在e中收集,为保证
在e中收集,为保证![]() 蒸气冷凝,应在水槽g中加入________.
蒸气冷凝,应在水槽g中加入________.
(4)![]() 遇到水蒸气强烈反应,甚至爆炸,所以d、e仪器及装入的物质都不能含有水.为除去氯气中的水分,c可装入的物质是________.
遇到水蒸气强烈反应,甚至爆炸,所以d、e仪器及装入的物质都不能含有水.为除去氯气中的水分,c可装入的物质是________.
A.碱石灰 B.浓硫酸 C.无水氯化钙
(5)氯气和白磷反应放出大量的热,为使曲颈甑d不致因局部过热而炸裂,实验开始前应在曲颈甑底部放少量____________.
(6)实验室白磷保存在水中,取出白磷后用滤纸吸干表面水分,浸入无水乙醇中片刻,再浸入乙醚中片刻即可完全除去水分.已知水与乙醇互溶,用上述方法除水分的原因是________________________________________________.
(7)为防止氯气污染空气,装置末端导出的气体最好用________进行净化处理.
[ ]
A.![]() 溶液 B.
溶液 B.![]() 溶液 C.饱和食盐水
溶液 C.饱和食盐水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com