
题目列表(包括答案和解析)
(8分)将2 mol H2O和2 mol CO置于1 L容器中,在一定条件下加热至高温,发生如下可逆反应:
2H2O(g) 2H2(g)+O2(g) 2CO(g)+O2(g)
2CO2(g)
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是________和________,或________和________。
(2)若平衡时O2和CO2的物质的量分别为n(O2)平=amol,n(CO2)平=b mol。试求n(H2O)平=________。(用含a、b的代数式表示)
(8分)将锌片和银片浸入100 mL 1mol·L―1稀硫酸中组成原电池。
(1)写出锌片和银片上的电极反应方程式?
(2)若该电池中两电极的总质量为6g,工作一段时间后,取出两极洗净干燥后称量质量为4.7g,试计算:①通过导线的电子的物质的量?②工作一段时间后,溶液中的H+的物质的量浓度?(设溶液的体积不变)
( 8分)将物质的量均为3.00mol物质A、B混合于5L容器中,发生如下反应 3A+B 2C,在反应过程中C的物质的量分数随温度变化如图所示:
2C,在反应过程中C的物质的量分数随温度变化如图所示: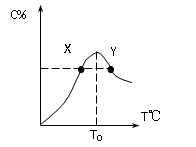
T0对应的反应速率V正和V逆的关系是_____(用含“>”“<”“=”表示,下同);
(2) 此反应的正反应为______热反应;
(3) X、Y两点A物质正反应速率的大小关系是______________;
(4) 温度T<T0时,C%逐渐增大的原因是________________________;
(5) 若Y点的C的物质的量分数为25%,则参加反应的A的物质的量为_______;若Y点时所耗时间为2min,则B物质的反应速率为__________。
(8分)将5.0LNaCl溶液和3.0LBaCl2溶液混和,设混和后总体积为8.0L,并测得NaCl物质的量浓度为0.50mol·L-1,BaCl2物质的量浓度为0.30mol·L-1。问:
(1)混合溶液中则Cl-物质的量浓度为多少?
(2)混和前NaCl溶液中NaCl的物质的量浓度为多少?
(8分)将6.50g锌投入200mL某浓度的盐酸中,锌和盐酸恰好完全反应。求:
(1)6.50g锌的物质的量;
(2)所用盐酸中HCl中的物质的量浓度;
(3)反应中生成的H2在标准状况下的体积。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com