
题目列表(包括答案和解析)
(10分)(1)可逆反应N2(g)+3H2(g) 2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为 。
2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为 。
(2)除电解法,工业炼镁还可采用硅热法(Pidgeon法)。即以煅白(CaO·MgO)为原料与硅铁(含硅75%的硅铁合金)混合置于密闭还原炉,1200℃下发生反应:
(CaO·MgO)(s) + Si(s) 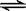 Ca2SiO4 (l) + 2Mg(g)
Ca2SiO4 (l) + 2Mg(g)
①已知还原性:Mg > Si,上述反应仍能发生的原因是______________________________
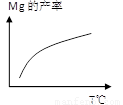
②由右图,推测上述反应正向为______(填“吸热”或“放热”)反应;平衡后若其他条件不变,将还原炉体积缩小一半,则达到新平衡时Mg(g)的浓度将______(填“升高” 、“降低”或“不变”)。
③若还原炉容积为400m3,原料中煅白质量为9.6 t,5小时后,测得煅白的转化率为50%,
计算这段时间Mg的生成速率 ___________ 。
(10分)(1)下面列出了几组物质,请将物质的合适组号填写在空格上。
同位素 同素异形体 同分异构体 同一种物质 。
①金刚石与“足球烯”C60; ②D与T; 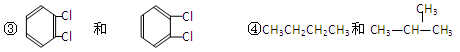
(2)写出下列反应方程式并注明反应类型
① ②
CH2=CH2 → CH3CH2OH → CH3COOCH2CH3
① 反应类型
② 反应类型
包括3小题,(共10分)
(1)1mol H2SO4中约含有 个H2SO4, mol H , mol O
(2)9.03×1023个CO2的物质的量是 mol,在标准状况下的体积 L, 质量是是 克。
(3)在100mL2mol/LH2SO4溶液中,H2SO4的质量是 克。H+的物质的量浓度为 。
(4)质量分数为36.5%、密度为1.18g/cm3的浓盐酸中HCl的物质的量浓度为 。
(14分)(1)(4分)将100.0g Na2CO3和NaHCO3固体混合物充分加热,使产生的水蒸汽和CO2全部通入足量的Na2O2中充分反应,产生11.2L的气体(气体体积已转算成标准状况下体积),则混合物中Na2CO3质量分数是 。
(2)(10分)200 mL 2.00 mol/L的Al2(SO4)3溶液中含有 mol Al2(SO4)3, Al3+的物质的量浓度为 ,SO42-的物质的量浓度为 ,含Al3+的物质的量为 ,质量为 。
(10分) (1)将一小块金属钠投入水中,发生反应的化学方程式为 ,请回答:可观察到的实验现象是_____________(填字母)。
a.钠沉到水底
b.钠熔成小球
c.小球四处游动
d.向反应后的溶液中滴加酚酞试剂,溶液变为红色
(2)在实验室中,通常将金属钠保存在 (填字母)。
a.水中 b. 煤油中 c. 四氯化碳中
(3)过氧化钠与水反应,化学方程式: 。
(4)过氧化钠与二氧化碳反应,化学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com