
题目列表(包括答案和解析)
研究化学反应原理对于生产生活是很有意义的。
(1)下列关于醋酸的叙述正确的是 (填写符号)。
a.等体积等pH的醋酸和盐酸完全被NaOH溶液中和,消耗NaOH的物质的量一样多
b.向醋酸溶液中加入一定量NaOH固体,溶液的导电性增强
c.加水稀释醋酸溶液,溶液中的所有离子浓度均减小
d.常温下,醋酸溶液中水的电离程度比纯水的小
(2)钢铁生锈现象随处可见,钢铁的电化腐蚀原理如图所示:
①写出石墨电极的电极反应式 ;
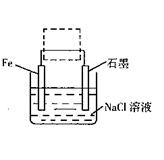
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改。
③写出修改后石墨电极的电极反应式 。
(3)①高炉炼铁过程中会发生反应:FeO(s)+CO(g) Fe(s)+CO2(g)。
Fe(s)+CO2(g)。
已知:Fe(s)+1/2O2(g)=FeO(s)△H= -272kJ·mol-1
C(s)+O2(g)=CO2(g) △H= -393.5kJ·mol-1
2C(s)+O2(g)=2CO(g) △H= -22lkJ·mol-1
则:①FeO(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)
△H= 。
②一定温度下,向某密闭容器中加人足量FeO,
并充人一定量的CO气体,反应过程中CO和CO2的
浓度与时间的关系如图所示则从开始至达到平衡过程中, (CO)= 。
(CO)= 。
(4)铁红是一种红色颜料,其成份是Fe2O3。将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加人一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为 。
研究化学反应原理对于生产生活是很有意义的。
(1)下列关于醋酸的叙述正确的是 (填写符号)。
a.醋酸俗名冰醋酸,是食醋的主要成分
b.向醋酸溶液中加入一定量NaOH固体,溶液的导电性增强
c.加水稀释醋酸溶液,溶液中的所有离子浓度均减小
d.常温下,醋酸溶液中水的电离程度减小
(2)牙釉质对牙齿起着保护作用,其主要成分为Ca5(PO4)3OH,该物质在水中存在沉淀溶解
平衡,试写出该物质的溶度积常数表达式Kap= 。
(3)钢铁生锈现象随处可见,钢铁的电化腐蚀原理
如图所示:
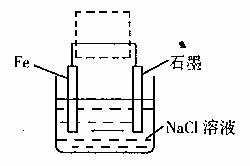
①写出石墨电极的电极反应式 ;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向。
③写出修改后石墨电极的电极反应式 。
 Fe(s)+CO2(g)。
Fe(s)+CO2(g)。 Fe(s)+CO2(g)
Fe(s)+CO2(g) (CO)= 。
(CO)= 。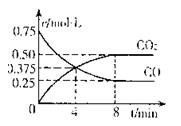
 (2010?潍坊一模)研究化学反应原理对于生产生活是很有意义的.
(2010?潍坊一模)研究化学反应原理对于生产生活是很有意义的.已知A、B、C、D为中学常见的气体单质,甲、乙、丙、丁为常见的化合物,甲的水溶液呈碱性。它们之间有如图所示的转化关系(部分产物及反应条件已略去)。

请回答:
 (1)乙的名称为 ,丙转化丁的离子方程式为 。
(1)乙的名称为 ,丙转化丁的离子方程式为 。
(2)实验室可通过多种方法制备甲,用右图所示装置收集甲,下列关于制取及收集甲实验的叙述正确的是 。
①甲气体不能用排水法收集
②实验室用丙一种药品可以制取甲
③右图的a为浸有稀H2SO4的棉花
|
(3)在A转化为甲的过程中,有右图所示的数据
(单位:mol/L)。在2min内A与D反应生成甲的速度V(甲)= ,2min末A的转化率为 。
(4)工业上通常以甲为原料制备HNO3。硝酸工业尾气中的NO和NO2对环境有污染,可用NaOH溶液吸收,尾气中NO与NO2按物质的量之比1:1被NaOH溶液吸收得到一种钠盐,该反应的化学方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com