
题目列表(包括答案和解析)
【提出猜想】同学们对溶液中Fe3+和![]() 之间的反应进行了猜想,提出了如下观点:
之间的反应进行了猜想,提出了如下观点:
Ⅰ、认为发生相互促进的水解反应,其离子反应方程式为:
2Fe3++3![]() +6H2O
+6H2O![]() 2Fe(OH)3(胶体)+3H2SO3
2Fe(OH)3(胶体)+3H2SO3
Ⅱ、认为发生氧化还原反应,其离子反应方程式为:
2Fe3++![]() +H2O
+H2O![]() 2Fe2++2H++
2Fe2++2H++![]()
【实验验证】为验证“猜想”,同学们实验如下:
(1)取一定量的Na2SO3固体配成Na2SO3浓溶液。
(2)取5 mL FeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,溶液颜色先由黄色变为红棕色,但无气泡产生,无沉淀生成;继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变成红褐色溶液。
(3)换用稀释的FeCl3和Na2SO3溶液重复上述实验,产生的现象完全相同。
(4)为判断红褐色溶液中含有Fe(OH)3从而证明猜想Ⅰ正确。①部分同学认为只要证明该体系为胶体即可,因此通过_____________现象设计实验方案,证明了其为Fe(OH)3胶体;
②部分同学从反证法的角度考虑,认为只要证明红褐色溶液中仍然有+3价的铁,可说明Fe3+没有被还原为Fe2+则猜想Ⅱ不正确,设计方案为,观察到,从而说明红褐色溶液中含有+3价的铁。
(5)另有部分同学认为只要证明红褐色溶液中含有![]() 可判断猜想Ⅱ正确,因此设计方案为_____________,观察到有白色沉淀生成_____________。
可判断猜想Ⅱ正确,因此设计方案为_____________,观察到有白色沉淀生成_____________。
【解释结论】综合(4)(5)考虑,Fe3+与![]() 的反应类型为_____________。
的反应类型为_____________。
【实验反思】某学同认为(5)中![]() 来源不一定是被Fe3+氧化得到的,因此不能推断猜想Ⅱ正确。你是否赞成该同学的观点_____________(填“是”或“否”)。如果赞成,你对实验改进的建议_____________(如果不赞成,该问不必作答)。
来源不一定是被Fe3+氧化得到的,因此不能推断猜想Ⅱ正确。你是否赞成该同学的观点_____________(填“是”或“否”)。如果赞成,你对实验改进的建议_____________(如果不赞成,该问不必作答)。
【拓展探究】鉴于Na2CO3在组成上与Na2SO3相似,某同学在FeCl3溶液中加入Na2CO3溶液,马上观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是_____________;同学们交流后认为二者水溶液与氯化铁溶液反应的现象差别很大,除![]() 有较强的还原性而
有较强的还原性而![]() 没有还原性的原因外,还可能有的原因是__________________________。
没有还原性的原因外,还可能有的原因是__________________________。
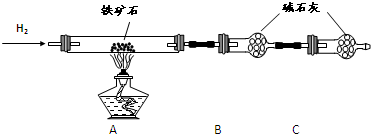
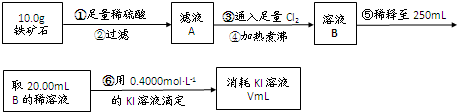

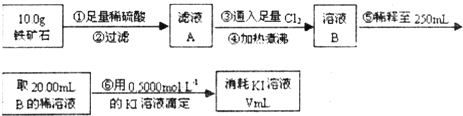
(10分)铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定
① 按上图组装仪器,检查装置的气密性;
② 将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③ 从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯;
④ 充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)装置C的作用为 。
(2)测的反应后装置B增重1.35g,则铁矿石中氧的质量百分含量为 。
(3)若将H2换成CO,则还需补充 装置。
(1)步骤④中煮沸的作用是 。
(2)下列有关步骤⑥的操作中说法正确的是 。
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测夜润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(3)若滴定过程中消耗0.5000mol·L−1的KI溶液20.00mL,则铁矿石中铁的质量百分含量为 。
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为 。
(10分)铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定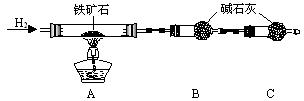
① 按上图组装仪器,检查装置的气密性;
② 将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③ 从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯;
④ 充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)装置C的作用为 。
(2)测的反应后装置B增重1.35g,则铁矿石中氧的质量百分含量为 。
(3)若将H2换成CO,则还需补充 装置。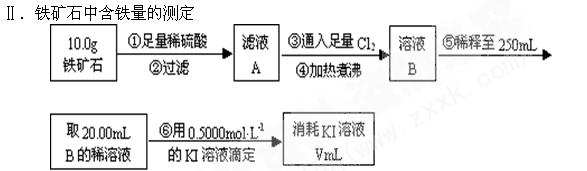
(1)步骤④中煮沸的作用是 。
(2)下列有关步骤⑥的操作中说法正确的是 。
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测夜润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(3)若滴定过程中消耗0.5000mol·L?1的KI溶液20.00mL,则铁矿石中铁的质量百分含量为  。
。
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com