下列两题分别对应于“物质结构与性质”和“实验化学”两个选修课程模块的内容,请你选择其中一题作答,如果两题全做,则按A题评分。

A.(12分)【物质结构与性质】
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
⑴科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体晶格能数据如下表:
晶体
| NaCl
| KCl
| CaO
|
晶格能/(kJ·mol-1)
| 786
| 715
| 3 401
|
4种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是
▲ 。
⑵科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示。
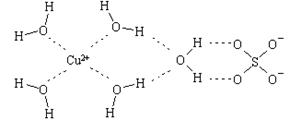
①写出基态Cu原子的核外电子排布式
▲ ;金属铜采用下列
▲ (填字母代号)堆积方式。
A B C D
②写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)
▲ 。
③水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响
▲ 。
④SO
42-的空间构型是
▲ 。
B.(12分)【实验化学】
硫酸亚铁铵的化学式为(NH
4)
2SO
4·FeSO
4·6H
2O,又名莫尔盐,是分析化学中常见的还原剂。某化学研究小组设计如下实验来制备莫尔盐并测定硫酸亚铁铵的纯度。
步骤一:铁屑的处理与称量。在盛有适量铁屑的锥形瓶中加入Na
2CO
3溶液,加热,过滤、洗涤、干燥、称量,质量记为
m1。
步骤二:FeSO
4的制备。将上述铁屑加入到一定量的稀H
2SO
4中,充分反应后过滤并用少量热水洗涤锥形瓶和滤纸。滤液及洗涤液完全转移至蒸发皿中。滤渣干燥后称重,质量记为
m2。
步骤三:硫酸亚铁铵的制备。准确称取所需质量的(NH
4)
2SO
4加入“步骤二”中的蒸发皿中,缓缓加热一段时间后停止,冷却,待硫酸亚铁铵结晶后过滤。晶体用无水乙醇洗涤并自然干燥,称量所得晶体质量。
步骤四:用比色法测定硫酸亚铁铵的纯度。
回答下列问题:
⑴步骤三中称取的(NH
4)
2SO
4质量为
▲ 。
⑵①铁屑用Na
2CO
3溶液处理的目的是
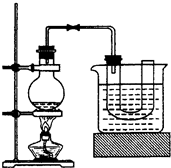
▲ 。制备FeSO
4溶液时,用右图装置趁热过滤,原因是
▲ 。
②将(NH
4)
2SO
4与FeSO
4混合后加热、浓缩,停止加热的时机是
▲ 。
③比色法测定硫酸亚铁铵纯度的实验步骤为:Fe
3+标准色阶的配制、待测硫酸亚铁铵溶液的配制、比色测定。标准色阶和待测液配制时除均需加入少量稀HCl溶液外,还应注意的问题是
▲ 。
④该实验最终通过
▲ 确定硫酸亚铁铵产品等级。



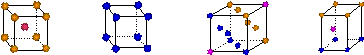
 研究性学习小组进行溴乙烷的制备及性质探究实验.
研究性学习小组进行溴乙烷的制备及性质探究实验.