
题目列表(包括答案和解析)
ATP(三磷酸腺苷)是体内生理活动所需能量的直接来源,故称之为“能量分子”。发现“能量分子”形成过程的科学家获得了1997年度的诺贝尔化学奖。ATP的结构如下:
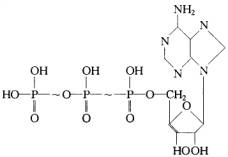
(1)ATP的分子式为___________________。
(2)ATP分子中含有两个P~O高能磷酸链,每水解裂开1molP~O键时,反应可释放约30.5KJ/mol能量。高能磷酸键的形成与断裂的反应过程即是“能量分子”传递能量的过程,转化关系为:
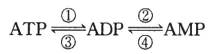
其中ATP与ADP、ADP与AMP的分子均相差80,则反应④是________。
A.释能反应
B.吸能反应
C.水解反应
D.磷酸化反应
(3)写出由AMP形成“能量分子”ATP的化学反应方程式,并标出能量的变化值:________。
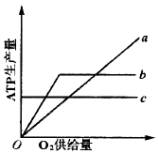
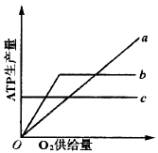
(4)如上图,能正确表示动物肌细胞内ATP产生量与O2,供给量之间关系的曲线是_______。
A.a
B.b
C.c
D.都不是
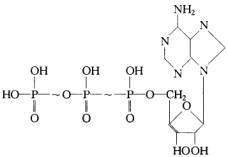
(1)ATP的分子式为___________________。
(2)ATP分子中含有两个P~O高能磷酸链,每水解裂开1molP~O键时,反应可释放约30.5KJ/mol能量。高能磷酸键的形成与断裂的反应过程即是“能量分子”传递能量的过程,转化关系为:
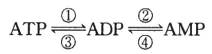
其中ATP与ADP、ADP与AMP的分子均相差80,则反应④是________。
A.释能反应
B.吸能反应
C.水解反应
D.磷酸化反应
(3)写出由AMP形成“能量分子”ATP的化学反应方程式,并标出能量的变化值:________。
(4)如上图,能正确表示动物肌细胞内ATP产生量与O2,供给量之间关系的曲线是_______。
A.a
B.b
C.c
D.都不是
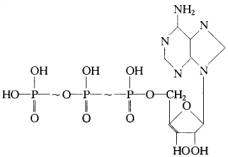
(1)ATP的分子式为___________________。
(2)ATP分子中含有两个P~O高能磷酸链,每水解裂开1molP~O键时,反应可释放约30.5KJ/mol能量。高能磷酸键的形成与断裂的反应过程即是“能量分子”传递能量的过程,转化关系为:
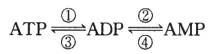
其中ATP与ADP、ADP与AMP的分子均相差80,则反应④是________。
A. 释能反应 B. 吸能反应
C. 水解反应 D. 磷酸化反应
(3)写出由AMP形成“能量分子”ATP的化学反应方程式,并标出能量的变化值:________。
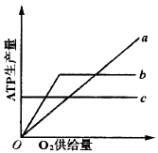
(4)如上图,能正确表示动物肌细胞内ATP产生量与O2,供给量之间关系的曲线是_______。
A.a
B.b
C.c
D.都不是
(10分)在本世纪20年代末,L.Pauling在大量含氧酸盐结构资料的基础上系统总结了关于离子化合物的五个规则。这些结构规则对诸如硅酸盐结构化学规律的总结和研究起了重大的推动作用。电价规则是鲍林五个规则的核心。它可表述为:在一个稳定的离子化合物结构中,每一负离子的电价等于或近似等于从邻近的正离子至该负离子的各静电键强度的总和,即ζ=![]() =
=![]() 式中:ζ为负离子的电荷;Si是i种正离子至每一配位负离子的静电键强度;Si定义为ωi/νi;ωi是正离子的电荷数;νi为其配位数。这一规则的物理基础在于:如在结构中正电位较高的位置安放电价较高的负离子时,结构会趋于稳定,而某一正离子至该负离子的静电键的强度ω/ν正是有关正离子在该处所引起正电位的量度。
式中:ζ为负离子的电荷;Si是i种正离子至每一配位负离子的静电键强度;Si定义为ωi/νi;ωi是正离子的电荷数;νi为其配位数。这一规则的物理基础在于:如在结构中正电位较高的位置安放电价较高的负离子时,结构会趋于稳定,而某一正离子至该负离子的静电键的强度ω/ν正是有关正离子在该处所引起正电位的量度。
1.化学式为Be3Al2[Si6O18]的绿柱石是含铍的矿物。结构中所有的Si4+均处于氧离子所组成的四面体空隙之中,键强Ssi-O= ,根据电价规则, 个Si-O键的键强和恰等于氧离子的电价数,决定了O2-可为 个硅氧四面体所公用。已知绿柱石中硅氧骨干外的Be2+分别处于O2-(硅氧骨干中的非公用氧离子)所组成的四面体的空隙中。硅氧骨干中每一个非公用的O2-各与一个Si4+、Be2+、Al3+相连,根据电价规则诸静电键强之和恰等于O2-之电价。则Al3+处于O2-(硅氧骨干中的非公用氧离子)所组成的_______体的空隙中。
2.以4价钒化合物VOSO4与盐酸羟胺为原料,在水溶液中以KOH调节pH≈4的条件下制得一种七配位的钒化合物[VO?(NH2O)2?(NH3O)?H2O]Cl。由晶体结构分析所得的键长算得诸键的键价如下:
键 | V-O(1) | V-O(2) | V-N(2) | V-O(3) | V-N(3) | V-O(4) | V-OH2 |
S | 1.811 | 0.639 | 0.581 | 0.707 | 0.596 | 0.526 | 0.220 |
产物中的钒为 价
 3.腺苷三磷酸(ATP)因其分子含有“高能键”(实为亚稳键)而在生物化学代谢过程中起着特别重要的作用。它可以通过水解反应使“高能”(即亚稳)磷酸键解离而起到能量传递的作用。已知正磷酸根PO43-中的P-O链长0.15nm,而ATP中的上述P-O键,已延伸至0.16nm,有力地佐证了此P-O亚稳键的起因。能否通过电价规则计算来证明。
3.腺苷三磷酸(ATP)因其分子含有“高能键”(实为亚稳键)而在生物化学代谢过程中起着特别重要的作用。它可以通过水解反应使“高能”(即亚稳)磷酸键解离而起到能量传递的作用。已知正磷酸根PO43-中的P-O链长0.15nm,而ATP中的上述P-O键,已延伸至0.16nm,有力地佐证了此P-O亚稳键的起因。能否通过电价规则计算来证明。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com