
题目列表(包括答案和解析)
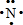
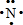


| ||
| 高温高压 |
| ||
| 高温高压 |
短周期元素X、Y、Z,Z是自然界中原子半径最小的元素;单质X2与Y2在放电的条件下反应生成A;X、Y、Z可以形成的化合物有 ZXY3、XZ4XY3等。
(1)写出X原子的电子式 ,画出Y的原子结构示意图 。
(2)写出X2与Z2化合生成XZ3的化学方程式 。
(3)将ZXY3的稀溶液和XZ3溶液混合,不可能出现的结果是 。
A.pH<7,且c(H+)>c(XY3-)>c(OH-)>c(XZ4+)
B.pH<7,且c(XY3-) + c(OH-)=c (H+) + c(XZ4+)
C.pH>7,且c (XZ4+)>c (OH-)>c (XY3-)>c (H+)
D.pH=7,且c (XZ4+) >c (XY3-)>c (H+)=c (OH-)
1. 写出ZXY3的稀溶液与过量铁粉反应的离子方程式 。
2. 当铜与ZXY3的浓溶液反应时,为防止有毒气体逸出污染空气,可将尾气通入NaOH溶液中,反应生成两种盐(物质的量相同)和水。写出其化学方程式 。
|
下列叙述正确的是 | |
A. |
铁与卤素(X2)反应的产物都是FeX3 |
B. |
氯化铁溶液中通入硫化氢气体生成的沉淀是Fe2S3 |
C. |
铁在氧气中燃烧可生成+2和+3价的氧化物 |
D. |
将含等物质的量的溶质的FeCl3、KSCN、HCl三种溶液混合后,不会产生沉淀 |
A.铁与卤素(X2)反应的产物都是FeX3
B.氯化铁溶液中通入硫化氢气体生成的沉淀是Fe2S3
C.铁在氧气中燃烧,可生成+2和+3价氧化物
D.将含有等物质的量溶质的FeCl3、KSCN、HCl三种溶液混合后,不会产生沉淀.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com