
题目列表(包括答案和解析)
(6分)在密闭容器中进行如下反应:mA(g)+nB(g)  pC(g),反应经5 min达到平衡,测得此时A的浓度减小了a mol·L-1,而C的浓度增加了2/3a mol·L-1,又知平均反应速率v(C)=2v(B)。
pC(g),反应经5 min达到平衡,测得此时A的浓度减小了a mol·L-1,而C的浓度增加了2/3a mol·L-1,又知平均反应速率v(C)=2v(B)。
(1)写出上述化学方程式中各物质的计量数:m=________,n=________,p=________
(2)压强一定时,C的百分含量(C%)与温度、时间(T表示温度,t表示时间)的关系如图所示。由此可知,该反应为 (填“吸热”或“放热”)反应。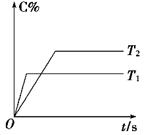
(3)该反应的平衡常数表示式为 ,升高温度,K值将 (填“增大”、“减小”或“不变”)。
(共8分)
在2 L恒容密闭容器中,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
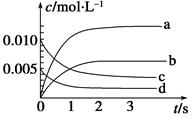
(6分)在一密闭的2 L容器中装有4 mol SO2和2 mol O2,在一定条件下开始反应。2 min末达到平衡且测得容器中有1.6 mol SO2 ,
(1)2 min末SO2的浓度_______________________________;
(2)2 min内SO2的平均反应速率________________________。
(3)达到平衡的标志是
①消耗2 mol SO2的同时生成2 mol SO3
② SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中,SO3的质量分数不再改变
(6分,每空1分)四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
|
元素 |
A |
B |
C |
D |
|
性质 结构 信息 |
室温下单质呈粉末状固体,加热易熔化。 单质在空气中燃烧,发出明亮的蓝紫色火焰。 |
单质常温、常压下是气体,能溶于水。 原子的M层有1个未成对的p电子。 |
单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 |
原子最外电子层上s电子数等于p电子数,等于电子层数。
|
(1)B元素在周期表中的位置 是___区 ,写出A离子的电子排布式
(2)写出C单质与水反应的离子方程式 ________
(3)A、B、C、 D四种元素的第一电离能由大到小的顺序 ________
(4)A、B两元素非金属性较强的是(写元素符号) ________ 。写出证明这一结论的一个实验事实
(6分)
在一个固定体积的密闭容器中,加入2 mol A和1 mol B,发生反应:2A(g)+B(g)3C(g)+D(g)达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度(用“大于”“小于”“等于”表示)。
(1) 加入1 mol A和1 mol B时,C的平衡浓度______ W mol·L-1。
(2) 加入2mol A、1mol B、3mol C、1mol D时,C的平衡浓度______W mol·L-1
(3) 加入3 mol C和1 mol D时,C的平衡浓度_________ W mol·L-1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com