
题目列表(包括答案和解析)
已知下列数据:
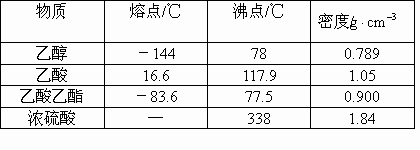
实验室制乙酸乙酯的主要步骤:
在30mL的大试管中按1:4:4的比例配制浓![]() 、乙醇和乙酸的混合液.
、乙醇和乙酸的混合液.
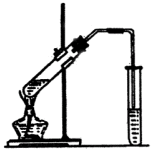
②如图5-22连接装置,使产生的蒸气经导管通到盛有4mL饱和![]() 溶液(加入滴酚酞试液的15mL试管中.)
溶液(加入滴酚酞试液的15mL试管中.)
③小火加热大试管中的混合物
④待小试管收集到约4mL产物时停止加热,撤出小试管并用力振荡,然后静置待其分层.
⑤分离纯净的乙酸乙酯
请回答下列问题:
(1)如何配制这一定比例的混合液________.
(2)写出该反应的化学方程式________反应中浓![]() 的作用是________.
的作用是________.
(3)在反应装置中,导气管出口的位置在![]() 液面上方2-3mm处,其理由是________;步骤③中为什么要小火加热________.
液面上方2-3mm处,其理由是________;步骤③中为什么要小火加热________.
(4)指出步骤④所观察到的现象是________.
原因与结论是________.
(5)为了提高乙酸乙酯的产率,甲、乙两同学分别设计了如图5-23、图5-24装置,乙同学待反应完毕后,放冷烧瓶中的液体,再用饱和![]() 溶液提取产物,你认为哪种装置合理?为什么?
溶液提取产物,你认为哪种装置合理?为什么?
| 1 |
| 3 |
| 1 |
| 3 |

| ||
| ||
| S2O | 2- 3 |
| S4O | 2- 6 |
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管Ⅰ、Ⅱ | 无现象 | |
| ② | 往试管I中加入 |
无现象 | 证明不是以IO3-形式存在 |
| ③ | 往试管Ⅱ中加入 |
证明以I-形式存在 |
 某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气 中O2的体积百分数.
某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气 中O2的体积百分数.| pH | 2.0 | 5.5 | 6.0 | 6.5 | 7.0 | 8.0 |
| 液柱高度 | 0cm | 1.3cm | 8.5cm | 8.4cm | 8.5cm | 8.5cm |
| 形成稳定液柱时间 | 3.0min | 3.1 min | 5.1 min | 5.3 min | 15.6 min | 17.5 min |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com