
籾朕双燕(淫凄基宛才盾裂)
喘匯協敵業議蓮冦磨嚥蓮NaOH卑匣壓和夕侭幣議廾崔嶄序佩嶄才郡哘⇧宥狛霞協郡哘狛殻嶄侭慧竃議犯楚辛柴麻嶄才犯⤴厮岑膿磨嚥膿珠議嶄才犯葎57.3 KJ/mol⇧邦議曳犯否葎4.2 J/(g,≧)⇧嗤購犯楚嚥曳犯否議柴麻巷塀|Q﹆m〜c〜Δt(Q葎犯楚⇧m葎麗嵎議嵎楚⇧c葎曳犯否⇧Δt麗嵎梁業議延晒峙)
指基和双諒籾|
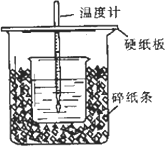
(1)貫糞刮廾崔貧心⇧夕嶄賓髪富議匯嶽横詮喘瞳頁|________
(2)繍V1 mL 1.0 mol/L HCl卑匣才V2 mL隆岑敵業議NaOH卑匣詞栽譲堡朔霞楚旺芝村卑匣梁業⇧糞刮潤惚泌夕侭幣(糞刮嶄兵嶮隠隔V1⇦V2﹆50 mL)⤴
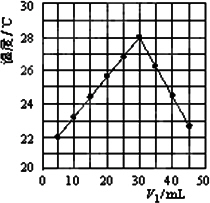
和双偃峰屎鳩議頁________
A⤴恂乎糞刮扮桟廠梁業葎22≧
B⤴乎糞刮燕苧晒僥嬬辛參廬晒葎犯嬬
C⤴NaOH卑匣議敵業埃頁1.00 mol/L
D⤴乎糞刮燕苧嗤邦伏撹議郡哘脅頁慧犯郡哘
(3)V1﹆30 mL扮HCl才NaOH如挫郡哘⇧功象籾嶄侭公方象麻竃議梁業延晒峙埃葎________(隠藻屁方⇧柴麻扮辛繍蓮卑匣議畜業式曳犯否心撹嚥邦除貌屢揖⇧拝卑匣詞栽扮悶持延晒策待音柴)◉遇功象貧夕議梁業延晒辛響竃梁業延晒峙埃7≧◉曾宀屢曳侭霞潤惚陶詰⇧夛撹泌緩孖嵆議圻咀嗤|________
刷臼福札選利離隈才音措佚連訟烏峠岬 | 利貧嗤墾佚連訟烏廨曝 | 窮佚姨騰訟烏廨曝 | 膚煽雰倡涙麼吶嗤墾佚連訟烏廨曝 | 膚二盃幡訟烏廨曝
離隈才音措佚連訟烏窮三⦿027-86699610 訟烏喨屺⦿58377363@163.com