
题目列表(包括答案和解析)
①pH之和为14的硝酸和氢氧化钾溶液 ②pH之和为15的盐酸和氨水溶液 ③pH之和为14的醋酸和苛性钠溶液 ④pH之和为13的硫酸和氢氧化钡溶液
A.② B.①② C.②③ D.③④
为研究HA、HB溶液和MOH的酸碱性的相对强弱,某化学学习小组设计了以下实验:室温下,将pH=2的两种酸溶液HA、HB和pH=12的碱溶液MOH各1 mL,分别加水稀释到1 000 mL,其pH的变化与溶液体积的关系如图所示,根据所给数据,请回答下列问题:

(1)HA为________酸,HB为________酸(填“强”或“弱”)。
(2)若c=9:则
①稀释前HB溶液和MOH溶液等体积混合后,溶液中c(B-) ________c(M+) (填“>”或“<”或“=”)。
②稀释后的三种溶液中,由水电离的氢离子的浓度的大小顺序为_______________________________________________ (用酸、碱的化学式表示)。
③将稀释后的HA溶液和MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为________(填“大于”“小于”或“等于”)。
(3)若b+c=14,则MOH为________碱(填“强”或“弱”)。将稀释后的HB溶液和MOH溶液取等体积混合,所得混合溶液的pH________7(填“大于”“小于”或“等于”)。
 H2(g)+CO2(g) △H=-41.2kJ/mol ,制备CO2与H2 的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用。
H2(g)+CO2(g) △H=-41.2kJ/mol ,制备CO2与H2 的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用。
 CO2(g)+ 2H2O(l) ΔH1=-890.3 kJ/mol
CO2(g)+ 2H2O(l) ΔH1=-890.3 kJ/mol  H2O(l) ΔH2=-285.8 kJ/mol
H2O(l) ΔH2=-285.8 kJ/mol 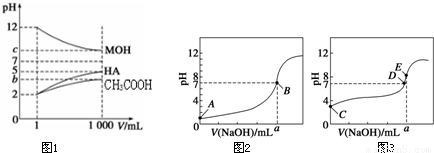

 CH3COOH+OH-
CH3COOH+OH- CH3COOH+OH-
CH3COOH+OH-湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com